МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
(МГС)
INTERSTATE COUNCIL FOR STANDARDIZATION, METROLOGY AND CERTIFICATION
(ISC)
МЕЖГОСУДАРСТВЕННЫЙ
СТАНДАРТ
МЕТОДЫ ИСПЫТАНИЙ ХИМИЧЕСКОЙ ПРОДУКЦИИ, ПРЕДСТАВЛЯЮЩЕЙ ОПАСНОСТЬ ДЛЯ ОКРУЖАЮЩЕЙ СРЕДЫОпределение комплексообразования в воде полярографическим методом
(OECD, Test No. 108:1981, MOD)
Издание официальное
|
Москва
Стандартинформ
2016 |
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2009 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены»
Сведения о стандарте
1 ПОДГОТОВЛЕН Межгосударственным техническим комитетом по стандартизации ТК 339 «Безопасность сырья, материалов и веществ» на основе собственного аутентичного перевода на русский язык международного документа, указанного в пункте 5
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии (Госстандарт)
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 22 июля 2015 г. № 78-П)
|
За принятие проголосовали: |
|
Краткое наименование страны по МК (ИСО 3166) 004—97 |
Код страны по МК (ИСО 3166) 004—97 |
Сокращенное наименование национального органа по стандартизации |
|
Армения |
AM |
Минэкономики Республики Армения |
|
Беларусь |
BY |
Госстандарт Республики Беларусь |
|
Казахстан |
KZ |
Госстандарт Республики Казахстан |
|
Киргизия |
KG |
Кыргызстандарт |
|
Россия |
RU |
Росстандарт |
|
Таджикистан |
TJ |
Т аджикстандарт |
|
4 Приказом Федерального агентства по техническому регулированию и метрологии от 12 октября 2015 г. № 1532-ст межгосударственный стандарт ГОСТ 33400-2015 введен в действие в качестве национального стандарта Российской Федерации с 1 сентября 2016 г.
5 Настоящий стандарт модифицирован по отношению к международному документу OECD, Test №108:1981 Complexformation ability in water (Polarographic method) [ОЭСР, Тест №108:1981 Комплексообра-зование в воде (полярографический метод)] путем изменения структуры. Сравнение структуры международного документа со структурой настоящего стандарта приведено в дополнительном приложении ДА.
Наименование настоящего стандарта изменено относительно наименования международного документа для приведения в соответствие с ГОСТ 1.5 (пункт 3.5).
Перевод с английского языка (еп).
Степень соответствия — модифицированная (MOD)
6 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
©Стандартинформ, 2016
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
Редактор И.И. Гпушкова Технический редактор В.Н. Прусакова Корректор М.И. Першина Компьютерная верстка А.Н. Золотаревой
Сдано в набор 01.02.2016. Подписано в печать 15.03.2016. Формат 60x84^. Гарнитура Ариал. Уел. печ. л. 1,40. Уч.-изд. л. 1,00. Тираж 35 экз. Зак. 742.
Издано и отпечатано во ФГУП «СТАНДАРТИНФОРМ», 123995 Москва, Гранатный пер., 4. www.gostinfo.ru info@gostinfo.ru
1 Область применения...................................................1
2 Термины и определения................................................1
3 Общие сведения.....................................................1
4 Принцип метода......................................................2
5 Достоверность испытания...............................................2
6 Стандартные вещества.................................................3
7 Процедура испытания..................................................3
8 Проведение испытания.................................................3
9 Данные и отчет о проведении испытания......................................4
Приложение ДА (справочное) Сопоставление структуры настоящего стандарта со структурой примененного в нем международного документа..........................5
Библиография........................................................6
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТМЕТОДЫ ИСПЫТАНИЙ ХИМИЧЕСКОЙ ПРОДУКЦИИ, ПРЕДСТАВЛЯЮЩЕЙ ОПАСНОСТЬДЛЯ ОКРУЖАЮЩЕЙ СРЕДЫОпределение комплексообразования в воде полярографическим методом
Testing of chemicals of environmental hazard. Determination of the complex formation ability in water
(polarographic method)
Дата введения —2016—09—01
1 Область применения
1.1 Настоящий стандарт устанавливает полярографический метод определения комплексообразования в воде.
1.2 Представленный метод основан на согласованном методе полярографии и может применяться только для чистых веществ, растворимость которых в воде выше 10-5 М.
1.3 Представленный метод не может использоваться для исследований комплексных соединений ртути.
2 Термины и определения
В настоящем стандарте применен термин с соответствующим определением:
2.1 потенциал полуволны £1/2 (half-wave potential): Потенциал в точке полярографической волны, при котором сила тока равна половине диффузионного тока.
3 Общие сведения
3.1 Способность новыххимических веществ кобразованию растворимых комплексов с металлами приводит к повышению доступности металлов для пищевых цепей. В иных случаях, например, при попадании в нерастворимые отложения, металлы становятся недоступными. Способность к комплексо-образованию имеет очень большое значение для таких металлов, как кадмий, медь, кобальт, хром, свинец и цинк, и может оцениваться с помощью полярографических методов, позволяющих определить константы устойчивости некоторых комплексных соединений.
3.2 Полярографический метод применяется для веществ с растворимостью в воде выше 10~5 М. Прямое измерение сдвига потенциала полуволны Е1/2 осуществляется при условии обратимой реакции на ртутном капельном электроде. С соответствующими модификациями испытание может проводиться также для необратимых процессов [6].
3.3 Два или более ионов могут быть определены последовательно, если их потенциалы полуволн различаются не менее чем на 0,4 В для одновалентных ионов и 0,2 В для двухвалентных ионов, при условии, что концентрации ионов примерно равны.
3.4 В случае если вещество образует несколько комплексов с ионом металла, то определение констант устойчивости промежуточных соединений также возможно, но, какправило, не является необходимым для оценки опасности для окружающей среды. При работе с сильными комплексообразователями следует соблюдать осторожность для предупреждения перегрузки системы (т.е. ситуации, когда не все металлы находятся в форме комплексов).
Издание официальное
3.5 Исследуемые показатели и единицы измерения
3.5.1 Потенциал Е ртутного капельного электрода определяется по соотношению:
Е=е(1) nF [Ms]'
где Е° — стандартный потенциал электродов;
R — газовая постоянная;
Т — абсолютная температура;
п — число электронов, участвующих в электродном процессе;
F— константа Фарадея;
Ма\л Ms — концентрации простых металлов в амальгаме и на поверхности электрода соответственно.
Соотношение (1) предполагает, что коэффициенты диффузии свободных ионов металлов и комплексов являются равными.
3.5.2 Константа устойчивости (константа комплексообразования) в реакции комплексообразо-вания
Мп + рхь -> МХр (л - рЬ)\ (2)
определяется как
к_[МХр(п-рЬ)+] (3)
[Мп+][Хь~]р ’
где р — координационное число.
Константа устойчивости зависит от температуры и коэффициента диффузии.
3.5.3 Комбинируя приведенные выше соотношения (1) и (3), получают следующую зависимость, действительную для обратимого восстановления комплексных соединений при 25 °С:
И)
где Е1/2 — потенциал полуволны комплексного соединения;
Ет — потенциал полуволны иона металла в отсутствие комплексообразователей;
X— концентрация исследуемого вещества.
3.5.4 Единицей измерения потенциала полуволны Е1/2в системе СИ является вольт, В.
4 Принцип метода
Метод основан на том, что потенциалы восстановления ионов металлов в результате комплексообразования сдвигаются, как правило, в отрицательную сторону. Положительный сдвиг происходит, только если в растворе присутствует ион другого металла, который способен связывать избыток комплексообразующего агента. Потенциал в точке полярографической волны, при котором сила тока равна половине диффузионного тока, называется потенциалом полуволны Е1/2. Данный параметр является характерной константой для ионов каждого металла.
Степень сдвига Е1/2 в присутствии комплексообразующего агента зависит от концентрации ком-плексообразователя, а также от стабильности комплекса. Измерение Е1/2 как функции концентрации вещества позволяет определить формулы и вычислить константы устойчивости некоторых комплексов металлов. Предполагается, что сдвиг Е1/2 происходит полностью за счет комплексообразования без участия диффузионного потенциала.
5 Достоверность испытания5.1 Воспроизводимость
В стандартных условиях (особенно при работе с ионами металла в диапазоне концентраций от 10-3 до 10-4 М) воспроизводимость метода составляет + 2 %. Температурный коэффициент составляет примерно 1,5 %—2,0 % на 1 °С. Следовательно, для точного измерения требуется контроль температуры с точностью до + 0,2 °С.
ГОСТ 33400-2015
5.2 Чувствительность
Чувствительность зависит от конкретной процедуры испытания. Как правило, метод позволяет определять концентрации ионов металлов ниже 10-5 М.
5.3 Специфичность
Метод может использоваться для веществ, способных образовывать стабильные водные растворы при концентрациях выше 10-5 М.
5.4 Возможность стандартизации
Метод может быть стандартизирован.
5.5 Возможность автоматизации
Возможность автоматизации не оценивалась.
6 Стандартные вещества
6.1 Использование стандартных веществ во всех случаях при испытании нового вещества не требуется. Использование стандартных веществ необходимо для периодической калибровки метода и возможности сопоставления результатов в случае применения других методов.
6.2 В качестве стандартных веществ рекомендуется использовать следующие вещества:
- этилендиаминтетрауксусная кислота (ЭДТА);
- нитрилоуксусная кислота;
- тиогликолевая кислота;
- о-нитрофенол.
7 Процедура испытания7.1 Подготовка оборудования
Подробное описание полярографов представлено в [1] — [8].
7.2 Условия испытания
7.2.1 Используемая в капельном электроде ртуть должна быть технически чистой, прошедшей двойную перегонку. Перед использованием ртуть необходимо отфильтровать.
7.2.2 В тестируемый раствор добавляют необходимое количество буферного раствора [4]. За 10—15 мин до определения потенциальной кривой токового электрода необходимо проводить дезоксигенацию тестируемого раствора, используя азот высокой чистоты.
7.2.3 Тестируют как минимум четыре известные концентрации исследуемого химического вещества с известными концентрациями ионов металлов. Тестируемые растворы в целях удобства готовят непосредственно в кювете полярографа с помощью точной бюретки. Концентрация тестируемого вещества в растворе должна не менее чем в 25 раз превышать концентрацию ионов металла с тем, чтобы концентрация тестируемого вещества на поверхности электродов была фактически равна его концентрации в основном объеме раствора. Силу тока измеряют при приложенной разности потенциалов в диапазоне от минус 0,2 В до минус 1,0 В.
7.2.4 Для детектирования комплексов, образование которых происходит медленно, необходимо первоначально выдерживать тестируемые растворы в атмосфере азота в течение минимум 24 ч и для подтверждения окончания комплексообразования на момент основного испытания проводить предварительное тестирование достаточного количества проб.
7.2.5 Следует внимательно оценить необходимость применения буферных растворов и поверхностно-активных веществ для подавления полярографических максимумов в целях предупреждения нежелательного влияния на контролируемый химической реакцией ток, а также на наклон полярографической волны.
8 Проведение испытания
Испытание проводят при температуре (25 ±0,2) °С. Описание проведения испытания представлено в [1]—[8].
3
9 Данные и отчет о проведении испытания9.1 Обработка результатов
Константа устойчивости /(определяется экстраполяцией графика зависимости потенциала полуволны Е1/2 от log[X|P кзначеник>Х= 1,0 М. Если графикзависимости представляет собой прямую (наклон которой, следовательно, составляет 0,0591/п), то предполагается образование комплекса 1:1. Образование гладких кривых может быть вызвано необратимой реакцией или образованием двух или более комплексов, находящихся в равновесии друг с другом. В последнем случае для постадийного расчета констант комплексообразования необходимо использовать метод де Форда и Хьюма [8].
9.2 Отчет о проведении испытания
Отчет о проведении испытания для каждого исследуемого металла должен содержать значение потенциала полуволны Е1/2, координационное число р и значение общей константы устойчивости.
Кроме того, в отчете о проведении испытания следует указать:
- тип поляризуемого микроэлектрода, тип стандартного электрода и, в случае использования ртутного капельного электрода, скорость потока в миллиграммах в секунду и время капания;
- использование ИК коррекции;
- использование подавителей максимумов;
- поддерживающий электролит;
- буферный раствор;
- температуру, при которой проводилось измерение;
- общую ионную силу тестируемого раствора;
- используемую процедуру испытания (метод с пилотным ионом, метод добавок или т. п.);
- технические трудности, возникавшие при проведении испытания;
- оценкуточности;
- используемый полярографический метод (например, DC, АС полярография, полярография с однократной разверткой, радиочастотная полярография или квадратно-волновая полярография).
9.3 Интерпретация и оценка результатов
9.3.1 Установленные константы устойчивости новых веществ сравниваютс приведенными в литературе значениями констант устойчивости стандартных веществ (раздел 6) и, следовательно, используют для оценки силы их комплексообразующей способности.
9.3.2 Испытание имеет физический смысл, если
a) значение константы устойчивости является положительным и
b) стандартная ошибка меньше, чем полученное значение константы (в качестве критерия используется f-тест).
9.3.3 Если данные не являются статистически значимыми, то следует использовать методы, основанные на других физико-химических принципах, такие как спектрофотометрия или спектроскопия ядер-но-магнитного резонанса.
4
ГОСТ 33400-2015
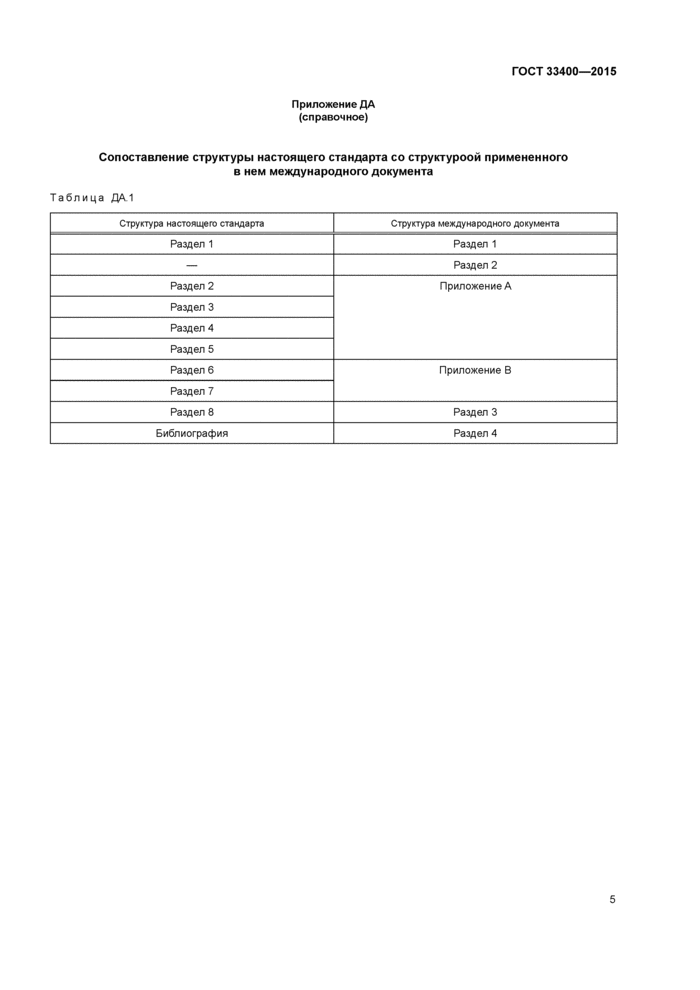
Приложение ДА (справочное)
Сопоставление структуры настоящего стандарта со структурой примененного в нем международного документа
|
Таблица ДА.1 |
|
Структура настоящего стандарта |
Структура международного документа |
|
Раздел 1 |
Раздел 1 |
|
— |
Раздел 2 |
|
Раздел 2 |
Приложение А |
|
Раздел 3 |
|
Раздел 4 |
|
Раздел 5 |
|
Раздел 6 |
Приложение В |
|
Раздел 7 |
|
Раздел 8 |
Раздел 3 |
|
Библиография |
Раздел 4 |
|
5
ГОСТ 33400-2015
Библиография
[1] A.I. Vogel and J. Basset, Vogel’s Textbook of Qualitative Inorganic Analysis, Chapter XIX, 4th Ed., Wiley, New York (1978) (А.И. Фогель и Д. Бассет , Учебное пособие «Качественный неорганический анализ», глава XIX, 4-е изд., М., Нью-Йорк(1978))
[2] D.R. Crow, J.V. Westwood, «The Study of Complexed Metal Ions by Polarpgraphic Methods», Quart. Rev., 19, 51 (1965) (Д.Р.Кроу, Д.Ж. Вествуд «Изучение комплексных соединений металлов полярографическим методом». кварт, откр., 19,51 (1965))
[3] Н. Irving «The Stability of metal Complexes and their Measurement Polagraphically», in Advances in Polarography— Proceedings of the 2nd International Congress, I.S.Langmuir(ed.), Pergamon Press (1960) (X. Ирвинг «Стабильность комплексов металлов и их измерения полярографией» Достижения в полярографии — 2-й Международный конгресс, (ред.), Пергамон Пресс (1960)
[4] D.D. Perrin, В. Dempsey, Bufferfor pH and Metal Ion Controls, Chapman and Hall, London (1974)
[5] «Stability Constants of Metal-ion Complexes», PartB: Organic Ligands, Compiled by D.D. Perrin, IUPAC Publication on Chemical Data Series, No. 22, Pergamon Press (1979)
[6] B. Grabaric, M. Tkalcec, I. Piljac, I. Filipovic, V. Simeon «Numerical Evaluation of Complex Stability Constants for Polarographic Data for Quasi-Reversible Processes», Anal. C him. Acta, 74,147, (1975).
[7] I. Piljac, B. Grabaric, I. Filipovic, «Improved Technique for Determination of Stability C onstants by Polarographic Method», J.EIectroanal. C hem. Interfacial Electrochem., 42,433 (1973) (И. Филипович, «Улучшенная методика определения стабильности полярографическим методом», 42,433 (1973))
[8] D.D. De Ford, D.N. Hume, «The Determination of Consecutive Formation Constants of Complex Ions from Polarographic Data», J. Amer. Chem. Soc., 73,532 1 (1951 )(Д.Д. Де Форд, Д. Н.Хьюм, «Определение последовательности образования постоянных комплексных ионов из полярографических данных» , Ю. Амер. хим. соц., 73, 532 1 (1951))
6
УДК 658.382.3:006.354 МКС 13.020.01 MOD
Ключевые слова: методы испытаний, химическая продукция, определение, комплексообразование, вода, полярографический метод
7