МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
(МГС)
INTERSTATE COUNCIL FOR STANDARDIZATION, METROLOGY AND CERTIFICATION
(ISC)
МЕЖГОСУДАРСТВЕННЫЙ
СТАНДАРТ
ПРОДУКЦИЯ СОКОВАЯОпределение содержания гесперидина и нарингина методом высокоэффективной жидкостной хроматографии
Издание официальное
Москва
Стандартинформ
2018
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены в ГОСТ 1.0-2015 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2015 «Межгосударственная система стандартизации. Стандарты межгосударственные. правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия. обновления и отмены»
Сведения о стандарте
1 РАЗРАБОТАН Некоммерческой организацией «Российский союз производителей соков» (РСПС) при участии Общества с ограниченной ответственностью «Люмэкс-маркетинг» (ООО «Люмэкс-маркетинг»)
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 30 августа 2018 г. № 111-П)
|
За принятие проголосовали: |
|
Краткое наименование страны по МК (ИСО 3166) 004—97 |
Код страны по МК (ИСО 3166)004—97 |
Сокращенное наименование национального органа по стандартизации |
|
Армения |
AM |
Минэкономики Республики Армения |
|
Беларусь |
BY |
Госстандарт Республики Беларусь |
|
Киргизия |
KG |
Кыргызстандарт |
|
Россия |
RU |
Росстандарт |
|
Узбекистан |
UZ |
Уэста ндарт |
|
4 Приказом Федерального агентства по техническому регулированию и метрологии от 12 октября 2018 г. № 755-ст межгосударственный стандарт ГОСТ 34461-2018 введен в действие в качестве национального стандарта Российской Федерации с 1 ноября 2019 г.
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
©Стандартинформ, оформление. 2018
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
9 Обработка и оформление результатов измерений
9.1 Если подготовка пробы была проведена по 8.1.2. то массовую концентрацию гесперидина (на-рингина) в пробе С. мг/дм3. вычисляют по формуле
где Сх— массовая концентрация гесперидина (нарингина) (см. 8.2.2). мг/дм3;
V2 — вместимость мерной колбы, используемой при подготовке пробы по 8.1.2. см3 (25 см3);
О — коэффициент дополнительного разбавления подготовленной пробы по 8.2.3. Если подготовленная проба дополнительно не была разбавлена, то О = 1;
V3 — объем аликвоты исходной пробы, см3 (5 см3).
За результат измерений массовой концентрации гесперидина (нарингина) в пробе принимают среднеарифметическое значениеС. мг/дм3, результатов двух параллельных измерений и С2. мг/дм3. при выполнении условия
100.l^ii£ W (9)
где лотн — предел повторяемости (см. таблицу 2). %.
Результат измерений округляют до целого числа.
9.2 Если подготовка пробы была проведена по 8.1.3. то массовую долю гесперидина (нарингина) в пробе X. млн-1, вычисляют по формуле
у С, У2 Q mV3 '
где VA — объем подготовленной по 8.1.3 пробы, равный 50 см3; т — масса пробы, г.
За результат измерений массовой доли гесперидина (нарингина) в пробе принимают среднеарифметическое значение X. млн-1, результатов двух параллельных измерений X, и Х2. Mnn-’. при выполнении условия
где готн — предел повторяемости (см. таблицу 2). %.
|
Таблица 2 — Метрологические характеристики метода при Р = 0.95 |
|
Наименование
показателя |
Диапазон
измерений |
Границы
относительной
погрешности
±6.% |
Предел повторяемости (допускаемое относительное расхождение результатов двух параллельных измерений) % |
Предел воспроизводимости (допускаемое относительное расхождение результатов двух единичных измерений) Котн.% |
|
Гесперидин |
|
Массовая концентрация. мг/дм3 |
От 100 до 1000 в ключ |
13 |
8 |
18 |
|
Массовая доля, млн-1 |
От 500 до 5000 в ключ |
|
|
|
|
Нарингин |
|
Массовая концентрация, мг/дм3 |
От 30 до 1000 в ключ |
10 |
7 |
13 |
|
Массовая доля, млн-1 |
От 150 до 5000 в ключ |
|
|
|
|
Результат измерения округляют до целого числа.
При невыполнении условий (9) или (11) получают еще два результата измерений в соответствии с разделом 8 и затем устанавливают результат измерений в соответствии с ГОСТ ИСО 5725-6 (подраздел 5.2).
9.3 Результаты измерений регистрируют в протоколе испытаний согласно ГОСТ ИСО/МЭК17025 с указанием настоящего стандарта. В протоколе испытаний результат измерений представляют в следующем виде (с указанием компонента) _
(С ± Дс), мг/дм3 (Р = 0.95) (12)
<Х± Дх). млн-1 (Р= 0.95). (13)
где С(Х) — среднеарифметическое значение результатов двух параллельных измерений (см. 9.1 и 9.2). мг/дм3 (млн-1);
Дс — значение границ абсолютной погрешности измерений массовой концентрации для доверительной вероятности Р= 0.95. мг/дм3, вычисляемое по формуле
5 С
Л‘=100' <14>
где 6 — значение границ относительной погрешности измерений массовой концентрации (массовой доли) для доверительной вероятности Р= 0,95 (см. таблицу 2), %;
Дх— значение границ абсолютной погрешности измерений массовой доли для доверительной вероятности Р= 0.95. млн-1, вычисляемое по формуле
(1S>
9.4 Результат измерений при содержании гесперидина (нарингина) менее нижней границы диапазона измерений представляют в протоколе в виде: «Менее Сн. мг/дм3» или «менее Хн. млн-1». Результат измерений при содержании гесперидина (нарингина) выше верхней границы диапазона измерений представляют в протоколе в виде:« Более Св. мг/дм3» или «более Хв, млн”1», где Сн (XJ и Св (Хв) — нижняя и верхняя границы диапазона измерений массовой концентрации (массовой доли) гесперидина (нарингина) (см. раздел 1).
9.5 Результаты измерений, полученные в двух лабораториях, признают совместимыми при выполнении условий
2COojs. (16)
С, +с2
где С, и С2 — результаты измерений массовой концентрации компонента в первой и второй лабораториях соответственно, полученные по 9.1, мг/дм3;
CD0 дБ — критическая разность, %, или
2 IX1-Х2 | ^о ?
Xi + Х2 '
где X, иХ2 — результаты измерений массовой доли компонента в первой и второй лабораториях соответственно. полученные по 9.2. млн-1.
Значение критической разности вычисляют по формуле
CDb. 95 = (18)
V пУ п2
где R0TH — предел воспроизводимости (см. таблицу 2), %; готн — предел повторяемости (см. таблицу 2). %;
п\ и п2 ~ числ0 параллельных измерений в первой и второй лабораториях соответственно.
Если условия (16) и (17) не выполняются, то лабораториям рекомендуется провести процедуры, предусмотренные ГОСТ 5725-6 (пункты 5.3.3 и 5.3.4).
10 Контроль качества результатов измерений
Контроль качества результатов измерений осуществляют, используя методы контроля стабильности среднеквадратического отклонения повторяемости и контроля стабильности среднеквадратического отклонения промежуточной прецизионности с применением контрольных карт Шухарта по ГОСТ ИСО 5725-6 (пункты 6.2.2. 6.2.3).
Периодичность контроля и процедуры контроля стабильности результатов измерений регламентируют в руководстве по качеству лаборатории в соответствии с ГОСТ ИСО/МЭК 17025 (пункт 4.2).
11 Требования безопасности
При выполнении измерений следует соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007, требования пожарной безопасности — по ГОСТ 12.1.004.
Требования электробезопасности при работе с приборами — по ГОСТ 12.1.019 и в соответствии с руководством по эксплуатации используемого оборудования.
12 Требования к квалификации операторов
К выполнению измерений и обработке результатов допускаются специалисты, имеющие высшее или специальное образование, опыт работы в химической лаборатории, изучившие руководство по эксплуатации жидкостного хроматографа и освоившие метод. Первое применение метода в лаборатории должно проводиться под руководством специалиста, владеющего теорией ВЭЖХ и имеющего практические навыки в этой области.
Ю
Приложение А (справочное)
Примеры хроматограмм
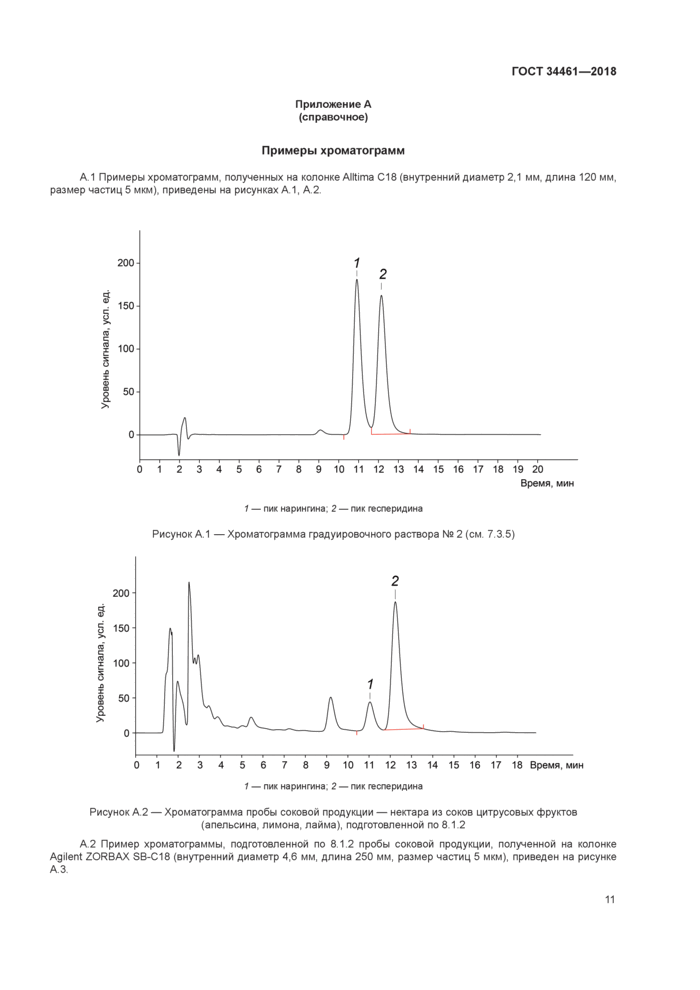
А 1 Примеры хроматограмм, полученных на колонке AJItima С18 (внутренний диаметр 2.1 мм. длина 120 мм. размер частиц 5 мкм). приведены на рисунках А 1, А 2
1 — пик нарингина. 2 — пик геспермдима Рисунок А 1 — Хроматограмма градуировочного раствора № 2 (см 7.3 5)
Рисунок А 2 — Хроматограмма пробы соковой продукции — нектара из соков цитрусовых фруктов (апельсина, лимона, лайма), подготовленной по 8 1 2
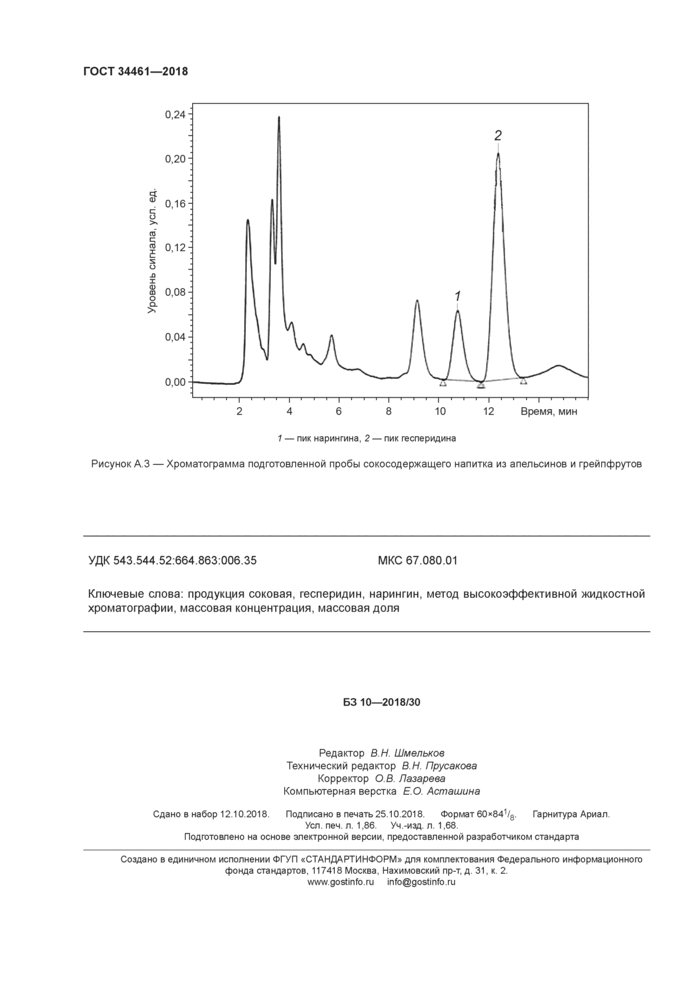
А 2 Пример хроматограммы, подготовленной по 8 12 пробы соковой продукции, полученной на колонке Agilent ZORBAX SB-C18 (внутренний диаметр 4,6 мм, длина 250 мм, размер частиц 5 мкм), приведен на рисунке АЗ.
1 — пи* наримгина. 2 — пик гесперидина Рисунок А 3 — Хроматограмма подготовленной пробы сокосодержащего напитка из апельсинов и грейпфрутов
УДК 543.544.52:664.863:006.35
Ключевые слова: продукция соковая, гесперидин. нарингин. метод высокоэффективной жидкостной хроматографии, массовая концентрация, массовая доля
БЗ 10—2018/30
Редактор В Н. Шмельков Технический редактор В Н Прусакова Корректор О В Лазарева Компьютерная верстка Е О Асташина
Сдано в набор 12 10 2018 Подписано в печать 2510 2018 Формат 60>84Ve. Гарнитура Ариал
Уел печ л 1.86 Уч-иэд л 1.68 Подготовлено на основе электронной версии, предоставленной разработчиком стандарта
Создано в единичном исполнении ФГУП «СТАНДАРТИНФОРМ» для комплектования Федерального информационного фонда стандартов. 117418 Москва. Нахимовский пр-т. д. 31. к. 2. www.gostKifo.ru info@gostinfo ги
Содержание
1 Область применения....................................................................................................................................1
2 Нормативные ссылки....................................................................................................................................1
4 Средства измерений, вспомогательное оборудование, реактивы, посуда и материалы
5 Отбор проб............................................................................................................................
6 Условия проведения измерений..........................................................................................
7 Подготовка к проведению измерений .................................................................................
8 Проведение измерений.........................................................................................................
9 Обработка и оформление результатов измерений.............................................................
10 Контроль качества результатов измерений.......................................................................
3 Сущность метода......
11 Требования безопасности.......................................................................................................................10
12 Требования к квалификации операторов ..............................................................................................10
Приложение А (справочное) Примеры хроматограмм ..............................................................................11
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
ПРОДУКЦИЯ СОКОВАЯ
Определение содержания гесперидина и нарингина методом высокоэффективной жидкостной
хроматографии
Juice products
Determination of hespendm and naringin content by HPLC method
Дата введения — 2019—11—01
1 Область применения
Настоящий стандарт распространяется на соковую продукцию (соки, концентрированные соки, нектары, сокосодержащие напитки), произведенную на основе или с добавлением цитрусовых фруктов (апельсина, грейпфрута, мандарина, лимона и лайма), и устанавливает метод высокоэффективной жидкостной хроматографии (далее — ВЭЖХ) для определения содержания (массовой концентрации и массовой доли) гесперидина и нарингина.
Диапазон измерений массовой концентрации нарингина в готовой соковой продукции (соки, нектары и сокосодержащие напитки) составляет от 30 до 1000 мг/дм3, а гесперидина — от 100 до 1000 мг/дм3.
Диапазон измерений массовой доли нарингина в концентрированных соках составляет от 150 до 5000 млн-1, а гесперидина — от 500 до 5000 млн-1.
Примечание — 1 млн-1 соответствует 1 мг/кг
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты:
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.019-79' Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
ГОСТ 61-75 Реактивы. Кислота уксусная. Технические условия
ГОСТ OIML R 76-1—2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия Часть 1. Метрологические и технические требования. Испытания
ГОСТ 1770-74 (ИСО 1042—83. ИС0 4788—80) Посуда мерная лабораторная стеклянная. Цилиндры. мензурки, колбы, пробирки. Общие технические условия
ГОСТ ISO 3696-2013" Вода для лабораторного анализа. Технические требования и методы контроля
ГОСТ 4204-77 Реактивы. Кислота серная. Технические условия
ГОСТ 5712-78 Реактивы. Аммоний щавелевокислый 1-водный. Технические условия
* В Российской Федерации действует ГОСТ Р 12.1.019-2009
** В Российской Федерации действует ГОСТ Р 52501-2005 (ИСО 3696 1987) «Вода для лабораторного анализа Технические условия».
Издание официальное
ГОСТ ИСО 5725-1-2003' Точность (правильность и прецизионность) методов и результатов измерений. Часть 1. Основные положения и определения
ГОСТ ИСО 5725-6-2003” Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ ИСО/МЭК 17025—2009 Общие требования к компетентности испытательных и калибровочных лабораторий
ГОСТ 20289-74 Реактивы. Диметилформамид. Технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 26313-2014 Продукты переработки фруктов и овощей. Правила приемки и методы отбора
проб
ГОСТ 28311-89 Дозаторы медицинские лабораторные. Общие технические требования и методы испытаний
ГОСТ 29227-91 (ИСО 835-1—81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
Примечание — При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя за текущий год Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку
3 Сущность метода
Метод основан на экстракции гесперидина и нарингина из проб соковой продукции смесью N.N-диметилформамида и водного раствора щавелевокислого аммония с последующим измерением массовой концентрации указанных соединений в экстракте методом ВЭЖХ с фотометрическим детектированием в ультрафиолетовой области спектра.
4 Средства измерений, вспомогательное оборудование, реактивы, посудаи материалы
4.1 Хроматограф жидкостный со спектрофотометрическим детектором, обеспечивающим проведение измерений при 287 нм или диодно-матричным детектором в диапазоне длин волн от 190 до 600 нм. снабженный программным обеспечением для сбора и обработки данных, со следующими метрологическими характеристиками:
-относительное среднеквадратическое отклонение выходного сигнала по высоте и площади пика — не более 3 %;
-относительное среднеквадратическое отклонение выходного сигнала по времени удерживания — не более 1.0%.
Предел детектирования гесперидина и нарингина (при соотношении сигнал/шум, равном трем) должен быть не более 0.2 мг/дм3.
Рекомендуется использование термостата колонок.
4.2 Колонка хроматографическая"', заполненная обращенно-фазовым сорбентом С18. обеспечивающая число теоретических тарелок по пикам гесперидина и нарингина не менее 3000.
4.3 Колонка защитная (предколонка), заполненная обращенно-фазовым сорбентом.
4.4 Весы неавтоматического действия специального класса точности с пределом допускаемой абсолютной погрешности измерений ± 0.0001 г. 1 2 3
4.5 Весы неавтоматического действия высокого класса точности по ГОСТ OIML R 76-1. пределом допускаемой абсолютной погрешности измерения ± 0.001 г.
4.6 Пипетки градуированные 2-1-2-1,2-1-2-2, 2-1-2-5 и 2-1-2-10 по ГОСТ 29227.
Примечание — Допускается использование дозаторов с метрологическими характеристиками, соответствующими ГОСТ 28311
4.7 Колбы мерные 2-25-2. 2-50-2, 2-1000-2 по ГОСТ 1770.
4.8 Цилиндры мерные вместимостью 50. 100. 250. 1000 см3. 2-го класса точности, исполнений 2 или 2а по ГОСТ 1770.
4.9 Центрифуга лабораторная с частотой вращения не менее 83 с-1 (5000 об/мин), обеспечивающая фактор разделения (g-фактор) не менее 1000.
4.10 Шкаф сушильный с диапазоном рабочих температур от 50 °С до 200 °С.
4.11 Насос лабораторный вакуумный, мембранный или водоструйный по ГОСТ 25336, обеспечивающий разрежение от 2.5 до 10 кПа.
4.12 Баня водяная с регулятором температуры, обеспечивающая поддержание температуры в диапазоне от 40 °С до 100 °С.
4.13 Стаканы любого типа исполнения 1 вместимостью 50.100 см3 по ГОСТ 25336.
4.14 Колбы плоскодонные П-1-1000-29/32 или конические Кн-1 -250-29/32, Кн-1-1000-29/32 по ГОСТ 25336.
4.15 Сосуды стеклянные с завинчивающимися крышками (виалы) с инертным материалом септы вместимостью от 10 до 20 см3.
4.16 Пробирки одноразовые из полимерного материала типа Эппендороф или аналогичные вместимостью от 1 до 2 см3.
4.17 Пробирки полимерные центрифужные конические с завинчивающейся крышкой вместимостью 15 см3.
4.18 Фильтры мембранные с диаметром пор 0,20 и 0,45 мкм.
4.19 Вода дистиллированная по ГОСТ 6709 или вода для лабораторного анализа по ГОСТ ISO 3696 1-й степени чистоты (далее — вода для анализа).
4.20 Ацетонитрил для жидкостной хроматографии (оптическая плотность при 200 нм относительно дистиллированной воды должна быть не более 0.05 единиц оптической плотности), ос. ч.
4.21 N.N-Диметилформамид по ГОСТ 20289. х. ч.
4.22 Аммоний щавелевокислый 1-водный по ГОСТ 5712. х. ч.
4.23 Кислота уксусная ледяная по ГОСТ 61. х. ч.
4.24 Кислота серная по ГОСТ 4204, х. ч. или ч. д. а.
4.25 Гесперидин' с массовой долей основного вещества не менее 95 %.
4.26 Нарингин” с массовой долей основного вещества не менее 95 %.
Допускается применение других средств измерений с метрологическими характеристиками, вспомогательного оборудования, посуды, материалов с техническими характеристиками не ниже вышеуказанных и химических реактивов аналогичной квалификации.
5 Отбор проб
Отбор проб соковой продукции — по ГОСТ 26313.
6 Условия проведения измерений
При подготовке к проведению измерений и проведении измерений в лаборатории соблюдают следующие условия:
- температура окружающего воздуха.................................(20 ± 5) °С:
- атмосферное давление...................................................от 84.0 до 106.7 кПа;
- влажность воздуха.........................................................не более 80 %.
В лабораторных помещениях не должно быть загрязненности воздуха рабочей зоны пылью и агрессивными веществами, должны отсутствовать вибрация или другие факторы, влияющие на результаты измерений.
* CAS 520-26-3 (CAS — код соединения в американской реферативной системе по химии (Chemical Abstracts).
•1 CAS 10236-47-2.
7 Подготовка к проведению измерений
7.1 Подготовка стеклянной посуды
Посуду для приготовления и хранения подвижной фазы моют только серной кислотой (см. 4.24) без применения других моющих средств, тщательно промывают водопроводной водой и ополаскивают водой для анализа.
Остальную стеклянную посуду моют горячей водой с моющим средством, тщательно ополаскивают водой для анализа и сушат в сушильном шкафу при температуре 105 X.
7.2 Приготовление вспомогательных растворов
7.2.1 Приготовление раствора уксусной кислоты молярной концентрации 0,2 моль/дм3
В мерную колбу вместимостью 1000 см3 помещают приблизительно 200 см3 дистиллированной воды, добавляют 12 см3 концентрированной уксусной кислоты, разбавляют дистиллированной водой до метки и перемешивают.
Срок хранения раствора в стеклянном сосуде при температуре (4 ± 2) X — 3 мес.
7.2.2 Приготовление подвижной фазы
Подвижную фазу готовят смешиванием 200 см3 ацетонитрила (см. 4 20) и 800 см3 раствора уксусной кислоты (см. 7.2.1) в плоскодонной колбе вместимостью 1000 см3 (см, 4.14).
Срок хранения подвижной фазы в стеклянном сосуде при температуре (4 ± 2) °С — 14 сут.
Перед использованием подвижную фазу дегазируют и фильтруют в соответствии с указаниями изготовителя хроматографа и (или) колонки.
Примечания
1 В зависимости от типа сорбента и типоразмера применяемых колонок допускается варьирование состава подвижной фазы с целью разделения пиков гесперидина и нарингина и их отделения от пиков компонентов матрицы пробы
2 Допускается приготовление иных объемов подвижной фазы в зависимости от потребности
7.2.3 Приготовление раствора щавелевокислого аммония молярной концентрации 0,025 моль/дм3
В химическом стакане вместимостью 50 или 100 см3 взвешивают (3.55 ± 0.05) г щавелевокислого аммония 1-водного (см. 4.22) и растворяют приблизительно в 30 см3 воды для анализа. Полученный раствор количественно переносят в мерную колбу вместимостью 1000 см3. Доводят до метки водой для анализа и тщательно перемешивают.
Срок хранения раствора в стеклянном сосуде при температуре (20 ± 5) X — 3 мес.
Примечание —Допускается изменять объем приготавливаемого раствора в зависимости от потребности
7.3 Приготовление градуировочных и контрольных растворов
7.3.1 Общие положения
Растворы гесперидина и нарингина следует хранить в темном месте при температуре от 2 °С до 6 X в герметичной посуде, исключающей возможность испарения растворителя и контакт раствора с материалами иными, чем стекло. Растворы каждой концентрации готовят по потребности.
7.3.2 Приготовление основного раствора гесперидина номинального значения массовой концентрации 500 мг/дм3
В мерную колбу вместимостью 50 см3 помещают (25.0±0.5) мг гесперидина (см. 4.25). добавляют 10 см3 N.N-диметилформамида (см 4.21), тщательно перемешивают до полного растворения (при необходимости нагревают на водяной бане при температуре от 40 X до 45Х). Содержимое колбы доводят до метки подвижной фазой, приготовленной по 7.2.2, и тщательно перемешивают.
Срок хранения раствора в условиях по 7.3.1 — 4 сут.
7.3.3 Приготовление основного раствора нарингина номинального значения массовой концентрации 1000 мг/дм3
В мерную колбу вместимостью 25 см3 помещают (25,0 ± 0,5) мг нарингина (см. 4.26), добавляют 5 см3 N.N-диметилформамида (см. 4.21) и перемешивают до полного растворения нарингина. Содержимое колбы доводят до метки подвижной фазой, приготовленной по 7.2.2, и тщательно перемешивают.
Срок хранения раствора в условиях по 7.3.1 — 4 сут.
7.3.4 Фактическое значение массовой концентрации гесперидина (нарингина) в основном раство-ре С^. мг/дм3. вычисляют по формуле
где М — масса гесперидина (нарингина). мг;
1000 — коэффициент согласования размерности единиц объема;
0 — массовая доля основного вещества в исходном реактиве, использованном для приготовления основного раствора (указано в паспорте изготовителя). %;
У, — объем основного раствора, см3;
100 — коэффициент для перевода массовой доли основного вещества из процентов в безразмерную величину.
7.3.5 Приготовление градуировочных растворов
7.3.5.1 Приготовление градуировочного раствора № 1
В стеклянный сосуд с завинчивающейся крышкой (виалу) вместимостью от 10 до 20 см3 помещают пипеткой или дозатором 2 см3 основного раствора гесперидина (см. 7.3.2) и 1 см3 основного раствора нарингина (см. 7.3.3), добавляют пипеткой или дозатором 7 см3 подвижной фазы, приготовленной по 7.2.2. и тщательно перемешивают.
Номинальное значение массовой концентрации компонентов в градуировочном растворе № 1 составляет 100 мг/дм3. Фактическое значение массовой концентрации компонентов С,, мг/дм3. вычисляют по формуле
С, = Сос* Voc”, (2)
Чр
где Сосн — фактическое значение массовой концентрации компонента в основном растворе (см. 7.3.4), мг/дм3;
УосН-объем основного раствора компонента, использованный для приготовления градуировочного раствора № 1. см3;
Уф — объем приготовленного градуировочного раствора № 1. см3 (10 с»л3).
Раствор используют в день приготовления.
7.3.5.2 Приготовление градуировочных растворов № 2—5
В стеклянные сосуды с завинчивающейся крышкой (виалы) вместимостью от 10 до 20 ал3 помещают пипеткой или дозатором градуировочный раствор № 1 (см. 7.5.3.1). добавляют пипеткой или дозатором подвижную фазу, приготовленную по 7.2.2 (ал. таблицу 1). и тщательно перемешивают.
|
Таблица 1 |
|
Номер
раствора |
Объем аликвоты градуировочного раствора № 1. см3 |
Объем подвижной фазы, приготовленной по 7 2 2, см3 |
Массовая концентрация (номинальное значение) гесперидина (нарингина). мг/дм3 |
|
2 |
4 |
6 |
40 |
|
3 |
2 |
8 |
20 |
|
4 |
1 |
9 |
10 |
|
5* |
0,5 |
9.5 |
5 |
|
* Раствор № 5 используют только при установлении градуировочной характеристики для нарингина |
|
Фактическое значение массовой концентрации компонента в приготовленном градуировочном растворе Су, мг/дм3 вычисляют по формуле
где С, — фактическое значение массовой концентрации компонента в градуировочном растворе № 1 (см. 7.3.5.1). мг/дм3;
V^ — объем аликвоты градуировочного раствора № 1. использованный для приготовления данного градуировочного раствора (см. таблицу 1). см3;
Vj — объем приготовленного градуировочного раствора, см3 (10 см3).
Растворы используют в день приготовления,
7.4 Подготовка хроматографа к работе
Включение и подготовку хроматографа к работе, вывод его на рабочий режим, включая кондиционирование колонки, а также промывку гидравлической линии хроматографа и выключение хроматографа по окончании работы осуществляют в соответствии с руководством по эксплуатации.
7.5 Условия хроматографического анализа
При проведении хроматографического анализа создают и поддерживают следующие условия:
-температура колонки — 25 °С (при наличии термостата колонок);
-длина волны детектирования при использовании спектрофотометрического детектора — 287 нм;
- объем дозирования пробы — полное заполнение дозирующей петли (от 10 до 20 мм3);
- режим элюирования — изократический. подвижная фаза — по 7.2.2;
- объемную скорость потока подвижной фазы определяют типоразмерами хроматографической колонки. Рекомендуемое значение составляет 1.0 см3/мин для колонок длиной 250 мм и внутренним диаметром 4.6 мм и 0,2 см3/мин —для колонок длиной 150 мм и внутренним диаметром 2,1 мм.
7.6 Градуировка хроматографа
Для градуировки хроматографа регистрируют по две хроматограммы градуировочных растворов № 1—5 (см. 7.3.5) и, используя программное обеспечение к хроматографу, находят площади пиков компонентов, а затем устанавливают градуировочную характеристику для каждого компонента в виде функциональной зависимости площади пика от массовой концентрации компонента.
Градуировку проводят при освоении метода и далее — при смене оборудования, колонок, условий хроматографического анализа, при значительном изменении параметров хроматографического процесса (времени удерживания, эффективности, разрешения и асимметрии пиков), после ремонта хроматографа или при неудовлетворительных результатах контроля стабильности градуировочной характеристики (см. 7.7).
Примечание — После длительного перерыва в работе рекомендуется проверить стабильность градуировочной характеристики в нескольких точках (не менее двух) диапазона
7.7 Контроль стабильности градуировочной характеристики
Контроль стабильности градуировочной характеристики проводят ежедневно перед началом работы. используя заново приготовленный градуировочный раствор № 2.
Регистрируют не менее двух хроматограмм этого раствора, идентифицируют пики компонентов, внося при необходимости коррекцию времен удерживания и принимая во внимание параметры хроматографического процесса (эффективность колонки, время удерживания пиков, разрешение пиков, асимметрию пиков), и вычисляют массовую концентрацию гесперидина и нарингина с использованием действующей градуировочной характеристики.
Проверяют сходимость времен удерживания
^ -12\ S 0,05 ■ I (4)
где f, и t2 — время удерживания пика компонента на первой и второй хроматограммах соответственно, мин;
Т— среднеарифметическое значение времен удерживания и t2, мин.
Проверяют сходимость значений массовой концентрации компонентов
\Со-Ск2\<0,06Ск, (5)
где Ск1 и Ск2 — измеренное значение массовой концентрации компонентов в пробе для контроля по первой и второй хроматограммам соответственно, мг/дм3;
Ск — среднеарифметическое значение массовой концентрации Ск1 и Ск2. мг/дм3.
Градуировочная характеристика признается стабильной, если выполняется условие
1C,-CJ 5 0,08 -С*. (6)
где С, — фактическое значение массовой концентрации компонента в растворе, используемом для контроля стабильности градуировочной характеристики (см. 7.3.4), мг/дм3;
Ск0 — фактическое значение массовой концентрации компонента в растворе, используемом для контроля стабильности градуировочной характеристики (см. 7.3.4). мг/дм3.
Если условие (6) не выполняется, то процедуру контроля повторяют и при получении неудовлетворительного результата градуировку хроматографа проводят заново.
8 Проведение измерений
8.1 Подготовка проб к измерениям
8.1.1 Измерения проводят два раза в условиях повторяемости в соответствии с требованиями ГОСТ ИСО 5725-1.
8.1.2 Пробу соков, нектаров или сокосодержащих напитков интенсивно перемешивают и в две мерные колбы вместимостью 25 см3 (V2) отбирают аликвоты объемом 5 см3 (У-j) для проведения параллельных определений (см. 8.1.1).
Примечание — Аликвоты для параллельных определений должны быть отобраны одна за другой без задержки
В каждую мерную колбу вместимостью 25 см3 добавляют по 5 см3 раствора щавелевокислого аммония, приготовленного по 7.2.3. 5 см3 N.N-диметилформамида (см. 4.21). Содержимое колбы охлаждают до комнатной температуры, доводят до метки водой для анализа и тщательно перемешивают.
Нагревают в течение 10 мин на водяной бане при температуре от 90 СС до 100 °С и охлаждают до комнатной температуры.
Приблизительно 1.5 см3 полученного раствора помещают в одноразовую пробирку (см. 4.16). центрифугируют при скорости вращения 5000 об/мин (фактор разделения не менее 1000) в течение 5 мин и подвергают хроматографическому анализу по 8.2.
Примечание —Допускается замена центрифугирования фильтрованием через мембранные фильтры с диаметром пор 0.20 или 0.45 мкм Не допускается использование мембранных фильтров из полисульфона. так как они не устойчивы к ацетонитрилу, а также на основе политетрафторэтилена (PTFE) и его аналогов, поскольку эти материалы адсорбируют нарингин и гесперидин
8.1.3 Концентрированные соки предварительно разбавляют. В стакане вместимостью 50 см3 взвешивают от 4.5 до 5.5 г пробы концентрированного сока, добавляют от 5 до 10 см3 воды для анализа и перемешивают. Полученный раствор количественно (многократно ополаскивая стенки стакана водой для анализа) переносят в мерную колбу вместимостью 50 см3 (V4), доводят водой для анализа до метки и тщательно перемешивают. Затем проводят все процедуры, предусмотренные 8.1.2.
8.2 Проведение хроматографического анализа
8.2.1 Подготовленную по 8.1 пробу дозируют в хроматограф и ретстрируют две хроматограммы в тех же условиях, в которых были зарегистрированы хроматограммы градуировочных растворов (см. 7.5). На полученных хроматограммах идентифицируют пики определяемых компонентов, установив ширину окна идентификации 5 %, используя значения площадей пиков. Вычисляют значения массовой концентрации идентифицированных компонентов при помощи градуировочных характеристик, установленных по 7.6.
8.2.2 Проверяют выполнение условия (5). Если это условие выполняется, то в качестве значения массовой концентрации компонента в подготовленной по 8.1 пробе принимают среднеарифметическое полученных значений. Если условие не выполняется, находят и устраняют причины нестабильности, после чего ввод подготовленной пробы повторяют.
8.2.3 Если массовая концентрация гесперидина (нарингина) в подготовленной по 8.1.2 или 8.1.3 пробе превышает верхнюю границу диапазона градуировочной характеристики (100 мг/дм3). то подготовленную пробу разбавляют водой для анализа. Коэффициент разбавления О вычисляют по формуле
где Vp — объем разбавленной пробы, см3;
Va — объем аликвоты подготовленной по 8.1 пробы, взятый для разбавления, см3.
8.2.4 Примеры хроматограмм приведены в приложении А.
1
В Российской Федерации действует ГОСТ Р ИСО 5725-2-2002
2
В Российской Федерации действует ГОСТ Р ИСО 5725-6-2002
3
Например, хроматографические колонки Nucleosil 100-5С18 и Agilent ZORВАХ SB-C18 Данная информация приведена для удобства пользователей настоящего стандарта и не является поддержкой указанных продуктов Допускается использование аналогичных хроматографических колонок, в том числе с иными типоразмерами при соблюдении указанных требований 2