Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение массовой концентрации авермектиновых комплексов (аверсектина С и аверсектина Ci) в молоке и плазме животных методом высокоэффективной жидкостной хроматографии с флуоресцентным детектированием
Методические указания МУК 4.1.1919—04
ББК 51.23 060
060 Определение массовой концентрации авермектиновых комплексов (аверсектина С и аверсектина Ci) в молоке и плазме животных методом высокоэффективной жидкостной хроматографии с флуоресцентным детектированием: Методические указания.— М.: Федеральный центр госсанэпиднадзора Минздрава России, 2005.—16 с.
1. Разработчики: к. м. и. В. Г. Тер-Симонян, к. х. и. С. В. Авчук, к. б. и. Е. Б. Кругляк, д. б. и. Т. С. Новик (ООО НБЦ «Фармбиомед», Москва).
2. Рекомендованы к утверждению Комиссией по госсанэпиднормирова-нию Минздрава России.
3. Утверждены и введены в действие Руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации Г. Г. Онищенко 5 августа 2004 г.
4. Введены в первые.
ББК 51.23
Редакторы Аванесова Л. И., Максакова Е. И. Технический редактор Ломанова Е. В.
Подписано в печать 27.01.05 Тираж 3000 экз.
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека 127994, Москва, Вадковский пер., д. 18/20
Оригинал-макет подготовлен к печати и тиражирован Издательским отделом Федерального центра госсанэпиднадзора Минздрава РФ 113105, Москва, Варшавское ш., 19а Отделение реализации, тел. 952-50-89
О Роспотребнадзор, 2005 О Федеральный центр госсанэпиднадзора Минздрава России, 2005
2
МУК 4.1.1919—04
с временем удерживания 10—13 мин, соответствует сумме авермекти-нов А! и Вь
По результатам анализа образцов строят два калибровочных графика для производных А] + В] и А2 + В2 - на оси абсцисс откладывают количества авермектинов, нанесенных на колонку, а на оси ординат -площадь пиков, соответствующих авермектинам А! + В! и А2 + В2.
Примечание: содержание авермектинов Aj + и А2 + В2 для каждого градуировочного раствора рассчитывают исходя из их процентного содержания в каждом стандартном образце.
10.4. Подготовка проб к определению
10.4.1. Отбор проб
Пробы молока до начала анализа хранят в замороженном виде при минус 18—20 °С.
Кровь отбирают в пробирки с гепарином, центрифугируют. Плазму переносят в чистые пробирки, до начала анализа замораживают и хранят в холодильнике при минус 18—20 °С.
Допускается хранение проб молока и плазмы в течение 2 месяцев.
10.4.2. Экстракция и очистка образцов Плазма
1,0 см3 плазмы крови помещают в гомогенизатор, туда же добавляют 3 см3 смеси этиловый спирт-вода в соотношении 1:1. Обработку ведут при 4 500 об./мин в течение 10 мин. Из полученной эмульсии аверсектин экстрагируют этилацетатом 3 раза порциями по 8 мл. Экстракцию ведут в центрифужных пробирках при встряхивании с последующим центрифугированием. Этилацетатные экстракты (верхний слой) отбирают пипеткой и переносят в кругло до иную колбу вместимостью 100 мл. Этилацетат отгоняют в вакууме на роторном испарителе при температуре не выше 50 °С. Остаток растворяют в 4 см3 ацетонитрила (растворение ведут на ультразвуковой бане). Раствор переносят в широкую пробирку с притертой пробкой. Колбу, в которой производилась отгонка этилацетата, обмывают 2 см3 ацетонитрила и промывную фракцию также переносят в пробирку. Ацетонитрильный раствор 3—5 раз промывают 3—4 см3 гексана. Гексановые экстракты (верхний слой) отбирают пипеткой и отбрасывают, а ацетонитрильный раствор упаривают досуха. Сухой остаток используют для получения флуоресцирующих производных.
11
МУК 4.1.1919—04
Молоко
1,0 см3 молока помещают в гомогенизатор, туда же добавляют 5 см3 смеси ацетон-вода в соотношении 1 : 1 и обрабатывают в течение 5 мин при 4500 об./мин. Из полученной эмульсии аверсектин экстрагируют изооктаном. Экстракцию проводят дважды, беря на каждую экстракцию по 5 см3 изооктана. Экстракцию ведут при встряхивании и последующем центрифугировании. Экстракты объединяют и упаривают на роторном испарителе досуха. Остаток растворяют в 8 см3 ацетонитрила. Ацетонитрильный раствор трижды экстрагируют 5—10 см3 гексана. Гексановые экстракты отбрасывают. Ацетонитрильный раствор переносят в пробирку и упаривают в вакууме досуха. Сухой остаток используют для проведения дериватизации.
10.4.3. Проведение дериватизации и очистка образцов
Дериватизацию исследуемых проб и их очистку проводят так, как это описано для стандартных образцов (раздел 10.3.2 и 10.3.3).
Дериватизацию авермектинов исследуемого образца проводят одновременно с дериватизацией рабочих стандартов. Допускается хранение дериватизированных проб в холодильнике в течение 2 недель.
11. Выполнение измерений
Анализ включает не более 6 испытуемых образцов. Перед началом и в конце работы проводят анализ стандартного образца, чтобы убедиться в стабильности работы системы.
Объем наносимой на колонку пробы для всех объектов составляет 0,05 см3.
Условия проведения процесса хроматографирования описаны в разделе 10.3.4 для стандартного образца.
12. Обработка результатов
Для обработки результатов хроматографирования используется программа «Мультихром». На хроматограммах исследуемых образцов определяют площадь пиков производных по времени удерживания соответствующих пикам стандарта аверсектина.
По калибровочным графикам находят содержание авермектинов А! + В! и А2 + В2 в объеме инжектированной пробы испытуемого образца.
Содержание аверсектина в исследуемом образце рассчитывают по формуле:
МУК 4.1.1919—04
Х^в - концентрация аверсектина в образце, нг/см3;
СА В - содержание авермектинов А] + В! в объеме инжектированной пробы образца, определяют по графику, нг;
Са2в2 — содержание авермектинов А2 + В2 в объеме инжектированной пробы образца, определяют по графику, нг;
Vj - объем пробы, нанесенной на колонку, см3 (0,05 см3),
V2 - объем пробы, подготовленной для ВЭЖХ, см3 (0,1 см3);
V3 - объем пробы молока или плазмы, взятой для экстракции, см3;
К - коэффициент, учитывающий степень извлечения аверсектина для данного объекта (получен при постановке модельных опытов с внесением известных количеств аверсектина).
Для молока К = 0,90.
Для плазмы К = 0,7.
13. Оформление результатов измерений
Результаты измерений оформляют протоколом по форме.
Протокол № количественного химического анализа
1. Дата проведения анализа_
2. Место отбора пробы__
3. Название лаборатории_
4. Юридический адрес организации_
Результаты химического анализа
|
Шифр или № пробы |
Опре деляемый компонент |
Концентрация,
мг/м3 |
Погрешность измерения, % |
|
|
|
|
|
Ответственный исполнитель: Научный руководитель:
14. Контроль погрешности измерений
Значения полученных метрологических характеристик погрешности, норматива оперативного контроля точности и норматива оперативного контроля воспроизводимости приведены в прилож. 1, 2, 3 в виде зависимости от значения массовой концентрации анализируемого компонента в пробе С, которую определяют как среднеарифметическое результатов параллельных определений.
15. Нормы затрат времени на анализ
Для проведения анализов 3 образцов требуется 6 ч.
13
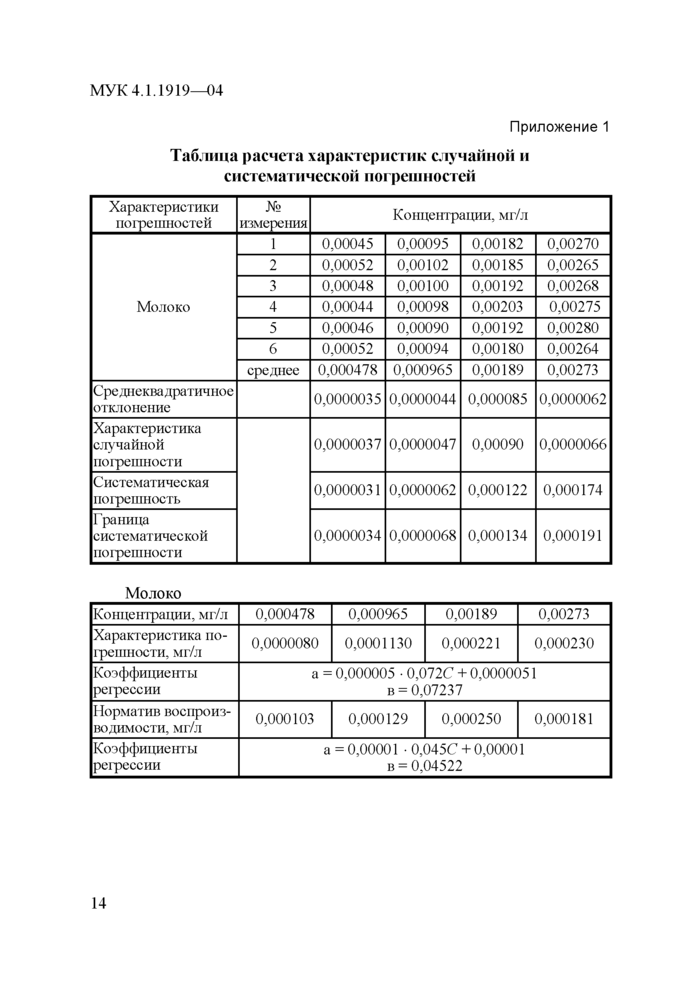
Приложение 1
Таблица расчета характеристик случайной и систематической погрешностей
|
Характеристики
погрешностей |
№
измерения |
Концентрации, мг/л |
|
Молоко |
1 |
0,00045 |
0,00095 |
0,00182 |
0,00270 |
|
2 |
0,00052 |
0,00102 |
0,00185 |
0,00265 |
|
3 |
0,00048 |
0,00100 |
0,00192 |
0,00268 |
|
4 |
0,00044 |
0,00098 |
0,00203 |
0,00275 |
|
5 |
0,00046 |
0,00090 |
0,00192 |
0,00280 |
|
6 |
0,00052 |
0,00094 |
0,00180 |
0,00264 |
|
среднее |
0,000478 |
0,000965 |
0,00189 |
0,00273 |
|
Среднеквадратичное
отклонение |
|
0,0000035 |
0,0000044 |
0,000085 |
0,0000062 |
|
Характеристика
случайной
погрешности |
|
0,0000037 |
0,0000047 |
0,00090 |
0,0000066 |
|
Систематическая
погрешность |
0,0000031 |
0,0000062 |
0,000122 |
0,000174 |
|
Г раница
систематической
погрешности |
0,0000034 |
0,0000068 |
0,000134 |
0,000191 |
|
Молоко |
|
Концентрации, мг/л |
0,000478 |
0,000965 |
0,00189 |
0,00273 |
|
Характеристика погрешности, мг/л |
0,0000080 |
0,0001130 |
0,000221 |
0,000230 |
|
Коэффициенты
регрессии |
а = 0,000005 • 0,072С + 0,0000051 в = 0,07237 |
|
Норматив воспроизводимости, мг/л |
0,000103 |
0,000129 |
0,000250 |
0,000181 |
|
Коэффициенты
регрессии |
а = 0,00001 • 0,045С + 0,00001 в = 0,04522 |
|
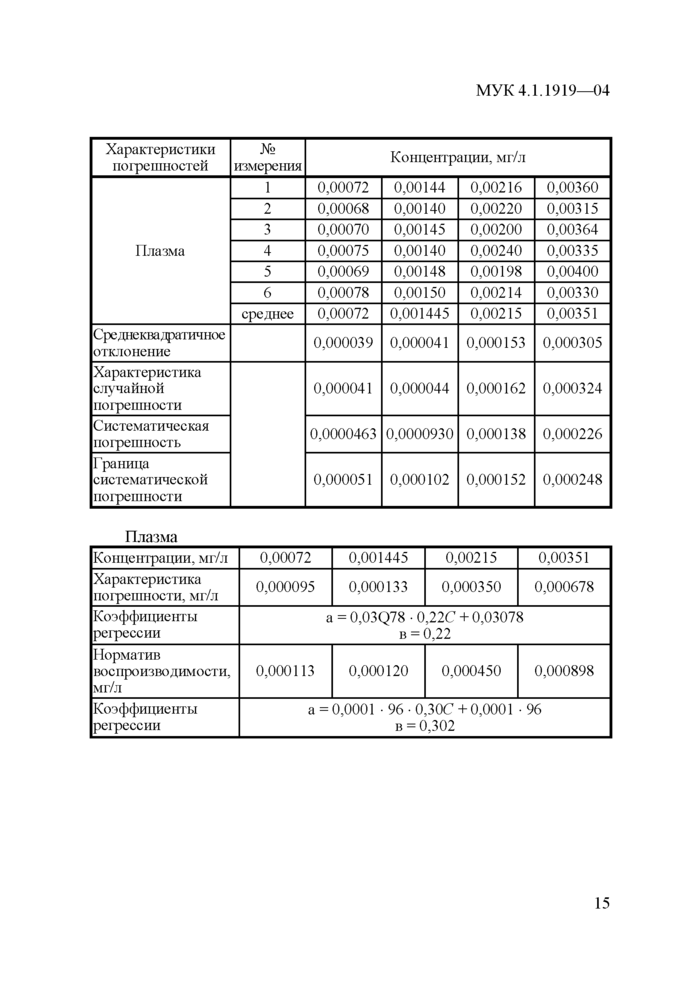
МУК 4.1.1919—04
|
Характеристики
погрешностей |
№
измерения |
Концентрации, мг/л |
|
Плазма |
1 |
0,00072 |
0,00144 |
0,00216 |
0,00360 |
|
2 |
0,00068 |
0,00140 |
0,00220 |
0,00315 |
|
3 |
0,00070 |
0,00145 |
0,00200 |
0,00364 |
|
4 |
0,00075 |
0,00140 |
0,00240 |
0,00335 |
|
5 |
0,00069 |
0,00148 |
0,00198 |
0,00400 |
|
6 |
0,00078 |
0,00150 |
0,00214 |
0,00330 |
|
среднее |
0,00072 |
0,001445 |
0,00215 |
0,00351 |
|
Среднеквадратичное
отклонение |
|
0,000039 |
0,000041 |
0,000153 |
0,000305 |
|
Характеристика
случайной
погрешности |
|
0,000041 |
0,000044 |
0,000162 |
0,000324 |
|
Систематическая
погрешность |
0,0000463 |
0,0000930 |
0,000138 |
0,000226 |
|
Г раница
систематической
погрешности |
0,000051 |
0,000102 |
0,000152 |
0,000248 |
|
Плазма |
|
Концентрации, мг/л |
0,00072 |
0,001445 |
0,00215 |
0,00351 |
|
Характеристика погрешности, мг/л |
0,000095 |
0,000133 |
0,000350 |
0,000678 |
|
Коэффициенты
регрессии |
а = 0,03Q78 • 0,22С + 0,03078 в = 0,22 |
|
Норматив
воспроизводимости,
мг/л |
0,000113 |
0,000120 |
0,000450 |
0,000898 |
|
Коэффициенты
регрессии |
а = 0,0001 • 96 • 0,30С + 0,0001 • 96 в — 0,302 |
|
15
|
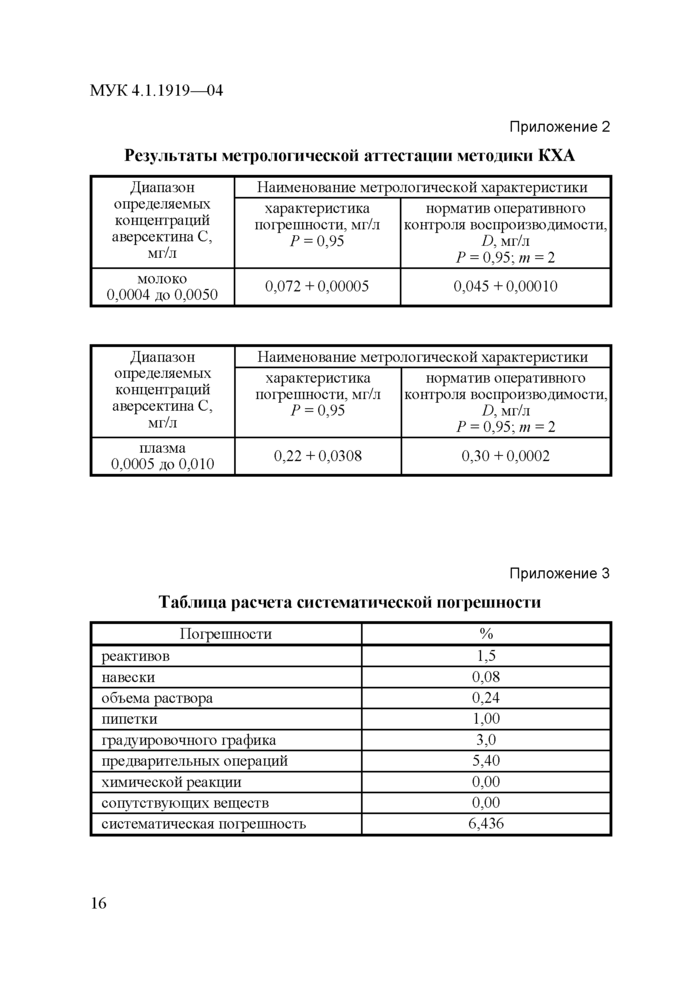
Приложение 2
Результаты метрологической аттестации методики КХА |
|
Диапазон определяемых концентраций аверсектина С, мг/л |
Наименование метрологической характеристики |
|
характеристика погрешности, мг/л Р = 0,95 |
норматив оперативного контроля воспроизводимости, Д мг/л Р = 0,95; т-2 |
|
молоко 0,0004 до 0,0050 |
0,072 + 0,00005 |
0,045 +0,00010 |
|
|
Диапазон определяемых концентраций аверсектина С, мг/л |
Наименование метрологической характеристики |
|
характеристика погрешности, мг/л Р = 0,95 |
норматив оперативного контроля воспроизводимости, Д мг/л Р - 0,95; т-2 |
|
плазма 0,0005 до 0,010 |
0,22 + 0,0308 |
0,30+0,0002 |
Приложение 3 Таблица расчета систематической погрешности
|
Погрешности |
% |
|
реактивов |
13 |
|
навески |
0,08 |
|
объема раствора |
0,24 |
|
пипетки |
1,00 |
|
градуировочного графика |
3,0 |
|
предварительных операций |
5,40 |
|
химической реакции |
0,00 |
|
сопутствующих веществ |
0,00 |
|
систематическая погрешность |
6,436 |
МУК 4.1.1919—04Содержание
1. Область применения...............................................................................................4
2. Общие положения...................................................................................................4
3. Физико-химические свойства, токсикологическая характеристика..................5
4. Погрешность измерений........................................................................................6
5. Метод измерений....................................................................................................6
6. Средства измерения, вспомогательные устройства, материалы,
реактивы, растворы................................................................................................7
7. Требования безопасности.......................................................................................8
8. Требования к квалификации оператора................................................................9
9. Условия измерений.................................................................................................9
10. Подготовка к выполнению измерений................................................................9
11. Выполнение измерений......................................................................................12
12. Обработка результатов.......................................................................................12
13. Оформление результатов измерений................................................................13
14. Контроль погрешности измерений....................................................................13
15. Нормы затрат времени на анализ......................................................................13
Приложение 1. Таблица расчета характеристик случайной и
систематической погрешностей....................................................14
Приложение 2. Результаты метрологической аттестации методики КХА..........16
Приложение 3. Таблица расчета систематической погрешности.........................16
3
УТВЕРЖДАЮ Руководитель Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Г лавный государственный санитарный врач
Г. Г. Онищенко
5 августа 2004 г.
Дата введения: с момента утверждения
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение массовой концентрации авермектиновых комплексов (аверсектина С и аверсектина Ci) в молоке и плазме животных методом высокоэффективной жидкостной хроматографии с флуоресцентным детектированием
Методические указания МУК 4.1.1919—04
1. Область применения
Методические указания по определению массовой концентрации авермектиновых комплексов (аверсектина С и аверсектина СД в молоке и плазме животных предназначены для проведения лабораторных исследований безопасности пищевой продукции учреждениями Госсанэпидслужбы Российской Федерации, а также для предприятий и учреждений, осуществляющих контроль качества пищевых продуктов в соответствии с Санитарно-эпидемиологическими правилами и нормативами «Гигиенические требования к безопасности и пищевой ценности пищевых продуктов», СанПиН 2.3.2.1078—01 и МДУ ГН 2.3.2.708—98 и аккредитованных в установленном порядке.
2. Общие положения
Аеерсектин С кАверсектин Cj - противопаразитарные препараты, представляющие собой комплексы близких в химическом отношении веществ - авермектинов, образуемых культурой Str. avermitilis. Отличия между ними заключаются в соотношении отдельных авермектиновых компонентов: так, основным компонентом аверсектина С является авермектин Вь тогда как основные компоненты аверсектина Q - авер-мектины А2 и В2.
4
МУК 4.1.1919—04
Аверсектины С и С\ являются действующими веществами ряда противопаразитарных лекарственных средств, используемых в ветеринарии (1 и 20 % аверсекта-2, аверсекта-3, мази аверсектиновой и др.).
Настоящие методические указания устанавливают хроматографическую методику количественного анализа молока и плазмы на содержание авермектинов после применения аверсектинсодержащих препаратов с нижним пределом измерения 0,001 мг/кг.
3. Физико-химические свойства, токсикологическая характеристика
Аверсектины С и Ci включают 4 гомологичных пары авермектинов: Аь А2; В]: В:. каждая из которых состоит из основного компонента, обозначаемого «а» и минорного - «в».
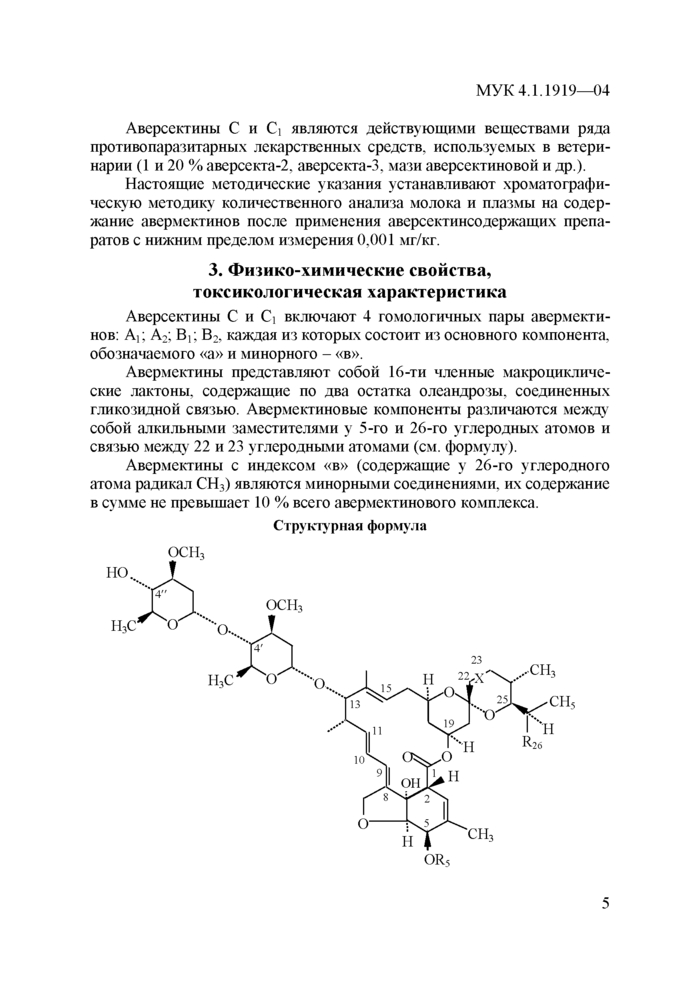
Авермектины представляют собой 16-ти членные макроцикличе-ские лактоны, содержащие по два остатка олеандрозы, соединенных гликозидной связью. Авермектиновые компоненты различаются между собой алкильными заместителями у 5-го и 26-го углеродных атомов и связью между 22 и 23 углеродными атомами (см. формулу).
Авермектины с индексом «в» (содержащие у 26-го углеродного атома радикал СН3) являются минорными соединениями, их содержание в сумме не превышает 10 % всего авермектинового комплекса.
Структурная формула
5
|
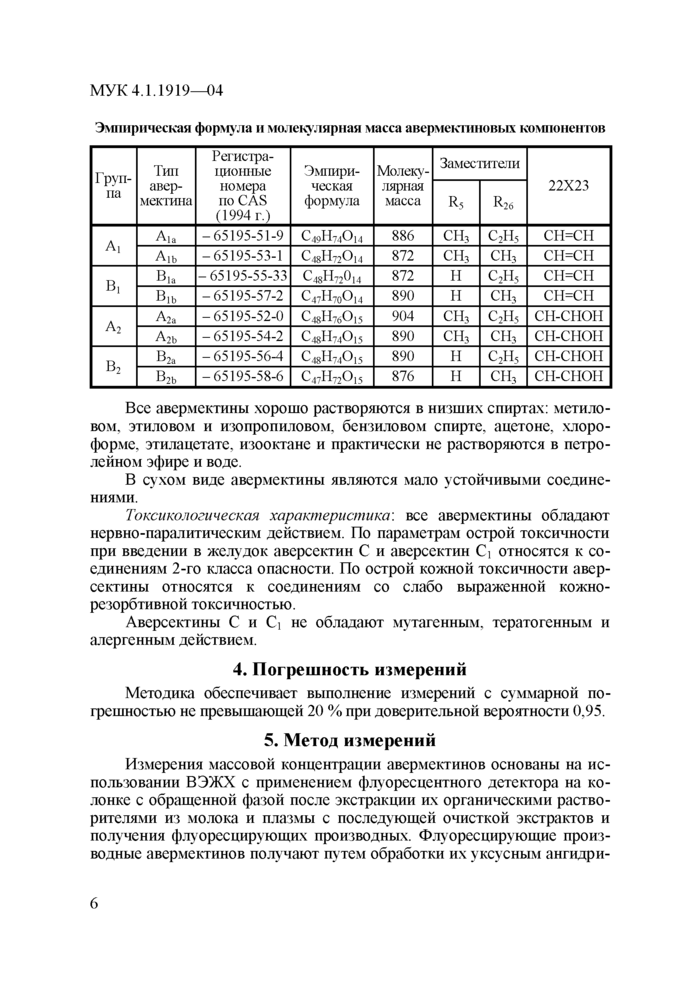
Эмпирическая формула и молекулярная масса авермектиновых компонентов |
|
Труп-
па |
Тип
авер-
мектина |
Регистрационные номера по CAS (1994 г.) |
Эмпири
ческая
формула |
Молеку-
лярная
масса |
Заместители |
22X23 |
|
r5 |
В26 |
|
Ai |
Aia |
-65195-51-9 |
С49Н74О14 |
886 |
СН3 |
С2Н5 |
сн=сн |
|
Aib |
-65195-53-1 |
C48H72Oi4 |
872 |
СН3 |
СН3 |
сн=сн |
|
Bi |
Bia |
-65195-55-33 |
|
872 |
Н |
С2Н5 |
сн=сн |
|
Bib |
-65195-57-2 |
С47Н70О14 |
890 |
Н |
СН3 |
сн=сн |
|
А2 |
Ага |
-65195-52-0 |
C48H760i5 |
904 |
СН3 |
с2н5 |
СН-СНОН |
|
Агь |
-65195-54-2 |
С48Н74О15 |
890 |
СН3 |
СН3 |
СН-СНОН |
|
в2 |
в2а |
-65195-56-4 |
C48H74Oi5 |
890 |
Н |
С2Н5 |
СН-СНОН |
|
В2ь |
-65195-58-6 |
C47H72Oi5 |
876 |
Н |
СН3 |
СН-СНОН |
|
Все авермектины хорошо растворяются в низших спиртах: метиловом, этиловом и изопропиловом, бензиловом спирте, ацетоне, хлороформе, этилацетате, изооктане и практически не растворяются в петро-лейном эфире и воде.
В сухом виде авермектины являются мало устойчивыми соединениями.
Токсикологическая характеристика: все авермектины обладают нервно-паралитическим действием. По параметрам острой токсичности при введении в желудок аверсектин С и аверсектин Ci относятся к соединениям 2-го класса опасности. По острой кожной токсичности авер-сектины относятся к соединениям со слабо выраженной кожно-резорбтивной токсичностью.
Аверсектины С и Ci не обладают мутагенным, тератогенным и алергенным действием.
4. Погрешность измерений
Методика обеспечивает выполнение измерений с суммарной погрешностью не превышающей 20 % при доверительной вероятности 0,95.
5. Метод измерений
Измерения массовой концентрации авермектинов основаны на использовании ВЭЖХ с применением флуоресцентного детектора на колонке с обращенной фазой после экстракции их органическими растворителями из молока и плазмы с последующей очисткой экстрактов и получения флуоресцирующих производных. Флуоресцирующие производные авермектинов получают путем обработки их уксусным ангидри-
МУК 4.1.1919—04
дом в присутствии N-метилимидазола на кипящей бане в течение часа. Указанные условия обеспечивают образование флуоресцирующих производных всех авермектинов, при этом в процессе реакции авермектины группы А! и В! дают производные, имеющие одинаковое строение, а так же как и авермектины группы А2 и В2. Хроматографическое разделение производных ведут на колонке с обращенной фазой, детекцию производных осуществляют по интенсивности флуоресценции при длинах волн возбуждения и эмиссии 365 и 470 нм соответственно.
При хроматографировании производные авермектинов элюируют из колонки двумя пиками: 1-й по времени удерживания пик соответствует сумме производных А2 и В2 (А2 + В2), второй - сумме производных группы А] и В] (Ai+Bi).
Примечание: в подобранных условиях хроматографирования производные минорных авермектинов имеют то же время удерживания, что и производные основных компонентов.
Таким образом, общее содержание авермектинового комплекса определяется суммой двух указанных пиков.
Минимальная определяемая концентрация производного, наносимая на колонку составляет 0,35 иг.
6. Средства измерения, вспомогательные устройства, материалы, реактивы, растворы
6.1. Средства измерения Аналитический хроматограф, Waters или аналогичный с флуоресцентным детектором, инжектором с объемом дозирующей петли -0,050 мл, с компьютерной системой обработки хроматографических данных (или с интегратором)
Весы аналитические 2-го класса точности ГОСТ 24104-88
Весы микроаналитические, точность взвешивания до 4-го десятичного знака, Chan (США) или аналогичные
Автоматические пипетки ТУ 64-1-3329—81
Колбы мерные, вместимостью 100 мл ГОСТ 1770-74
Цилиндры градуированные, вместимостью 100 мл ГОСТ 1770-74 Шприц Гамильтона (Швейцария)
6.2. Вспомогательные устройства
Центрифуга
Ультразвуковой диспергатор УЗДН-1М или аналогичный
7
МУК 4.1.1919—04
Миксер или гомогенизатор Холодильник
Колонка аналитическая Диасорб-130-С16Т 250 х 4, с размером частиц 6 мкм (фирма БиоХимМак, Россия) или аналогичная Гомогенизатор (Super-Mixer)
Патроны Диапак С1 (фирма БиоХимМак, Россия) Аппарат для упаривания - Vortex, Evaporater и др. Роторный испаритель с колбами Сушильный шкаф
Сцинтиляционные флаконы («Сигма», каталог 2001—2002 №....)
Баня водяная
63. Реактивы
Спирт этиловый Спирт метиловый
Ацетонитрил, хроматографически чистый или аналогичный 1-метилимидазол импортный;
Уксусный ангидрид, импортный;
Ацетон, чда Гексан, ч
Изооктан импортный
Стандартные образцы:
Аверсектин С: СОП (НБЦ «Фармбиомед») 20 %-ный раствор; содержа
ние аверсектина С и содержание авермектинов. Содержание авермектинов: (А^В^ и (А2+В2) в % по отношению к общему содержанию авермектинов (указано в паспорте)
Аверсектин Ср СОП (НБЦ «Фармбиомед») 20 %-ный раствор; содержание аверсектина Сх и содержание авермектинов. Содержание авермектинов: (Ai+Bi) и (А2+В2) в % по отношению к общему содержанию авермектинов (указано в паспорте)
7. Требования безопасности
7.1. При работе с реактивами соблюдают требования безопасности, установленные для работы с токсичными, едкими и легковоспламеняющимися веществами по ГОСТ 12.1.005-88
7.2. При проведении анализов горючих и вредных веществ соблюдают меры противопожарной безопасности по ГОСТ 12.1.004-76
МУК 4.1.1919—04
7.3. При выполнении измерений с использованием хроматографа соблюдают правила электробезопасности в соответствии с ГОСТ 12.1.019-79 и инструкции по эксплуатации прибора.
8. Требования к квалификации оператора
К выполнению измерений и обработке результатов допускают лиц с высшим и средним специальным образованием, имеющих навыки работы на жидкостном хроматографе.
9. Условия измерений
9.1. Приготовление растворов и подготовку проб к анализу проводят в нормальных условиях при температуре воздуха (20 ± 5) °С, атмосферном давлении 84—106 кПа и влажности воздуха не более 80 %.
9.2. Измерения на жидкостном хроматографе проводят в условиях, рекомендованных технической документацией к прибору.
10. Подготовка к выполнению измерений
10.1. Приготовление растворов
10.1.1. Готовят основной раствор стандартного образца Аверсек-тин С в этиловом спирте, таким образом, чтобы в 100 см3 раствора содержалось 10 мкг аверсектина (раствор № 1). Раствор хранят (в герметичной упаковке) в холодильнике 2 недели.
Так же поступают при использовании стандартного образца Авер-сектин Ci.
Примечание: использование того или другого стандартного образца обусловлено видом субстанции, содержащейся в препарате.
10.1.2. Раствор элюента готовят путем смешивания метилового спирта с водой в соотношении 98 : 2.
10.2. Подготовка прибора
Общую подготовку прибора осуществляют согласно инструкции по эксплуатации.
10.3. Установление градуировочной характеристики
10.3.1. Приготовление градуировочных растворов
Градуировочную характеристику, включающую взаимосвязь величины хроматографического сигнала и массу анализируемого вещества в хроматографируемом объекте, устанавливают по методу абсолютной калибровки с использованием серии градуировочных растворов.
МУК 4.1.1919—04
Из основного раствора № 1 готовят следующие разведения: в стеклянные пробирки с 0,5 см3 этилового спирта микрошприцем вносят по 0,005; 0,01; 0,02; 0,03; 0,05 и 0,1 см3 основного раствора, тщательно промывая микрошприц.
10.3.2. Получение флуоресцирующих производных (дериватизация)
Приготовленные растворы упаривают досуха в вакуумном сушильном шкафу при температуре 55 °С.
В пробирки с сухим остатком вносят при помощи градуированной микропипетки или микрошприца 0,005 см3 1-метилимидазола и 0,01 см3 уксусного ангидрида. Пробирки плотно закрывают, тщательно перемешивают, обрабатывают ультразвуком в течение 30 с.
Необходимо следить, чтобы в образцы перед проведением дерива-тизации не попала влага.
Пробирки с образцами помещают в кипящую водяную баню и выдерживают в течение 1 ч. По истечении этого времени образцы извлекают из водяной бани, охлаждают и доводят объем каждого образца до 0,5 см3, добавляя 0,485 см3 ацетонитрила.
10.3.3. Проведение твердофазной экстракции
Патрон Диапак С1 промывают смесью, содержащей 5,0 см3 ацетонитрила и 0,2 см3 ледяной уксусной кислоты, после чего на патрон наносят дериватизированную пробу. Пробирку, содержащую пробу, промывают 5,0 см3 ацетонитрила, промывку также наносят на патрон, далее патрон промывают 5,0 см3 ацетонитрила. Ацетонитрильный раствор упаривают в вакууме при 30—40 °С. Остаток растворяют в 0,1 см3 ацетонитрила. Подготовленную пробу используют для хроматографического анализа.
10.3.4. Проведение анализа ВЭЖХ и построение калибровочного графика
На колонку наносят по 0,05 см3 подготовленных дериватизирован-ных и очищенных стандартных образцов, содержащих 0,25; 0,5; 1; 1,5; 2; 2,5; 5 аверсектина.
Условия хроматографирования
Подвижная фаза - метиловый спирт-вода 98 : 2.
Скорость потока - 0,8 см3/мин. Давление - 120—160 атм.
Чувствительность детектора Range = 0,02.
Детектирование ведут по интенсивности флуоресценции при длинах волн возбуждения и эмиссии соответственно 365 и 470 нм.
На хроматограмме отмечают два пика: 1-й пик, с временем удерживания 8—10 мин соответствует сумме авермектинов А2 и В2; 2-й пик,