ЕВРАЗИЙСКАЯ ЭКОНОМИЧЕСКАЯ КОМИССИЯ КОЛЛЕГИЯ
РЕШЕНИЕ
«17» сентября 2019 г. № 158 г. Москва
О номенклатуре лекарственных форм и справочнике путей введения лекарственных препаратов
В соответствии со статьей 30 Договора о Евразийском экономическом союзе от 29 мая 2014 года, пунктами 4 и 7 Протокола об информационно-коммуникационных технологиях и информационном взаимодействии в рамках Евразийского экономического союза (приложение № 3 к указанному Договору) и руководствуясь Положением о единой системе нормативно-справочной информации Евразийского экономического союза, утвержденным Решением Коллегии Евразийской экономической комиссии от 17 ноября 2015 г. № 155, Коллегия Евразийской экономической комиссии решила:
1. Утвердить прилагаемые:
номенклатуру лекарственных форм (далее - номенклатура);
справочник путей введения лекарственных препаратов (далее -справочник);
Порядок ведения номенклатуры лекарственных форм и справочника путей введения лекарственных препаратов.
2. Включить номенклатуру и справочник в состав ресурсов единой системы нормативно-справочной информации Евразийского экономического союза.
3. Установить, что:
номенклатура и справочник применяются с даты вступления настоящего Решения в силу;
использование кодовых обозначений номенклатуры и справочника является обязательным при реализации общих процессов в рамках Евразийского экономического союза в сфере обращения лекарственных средств.
4. Настоящее Решение вступает в силу по истечении
30 календарных дней с даты его официального опубл!
Председатель Коллегии Евразийской экономической комиссии
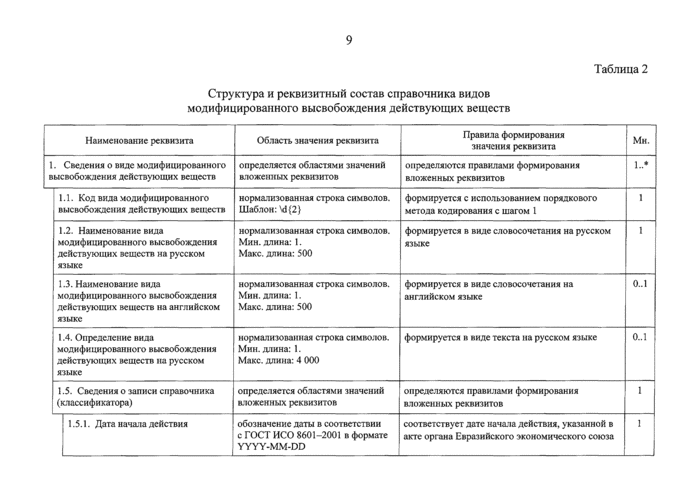
Структура и реквизитный состав справочника вилов модифицированного высвобождения действующих веществ
|
Таблица 2 |
|
Наименование реквизита |
Область значения реквизита |
Правила формирования значения реквизита |
Ми. |
|
1 |
|
Сведения о виде модифицированного |
определяется областями значений |
определяются правилами формирования |
1..* |
|
высвобождения действующих веществ |
вложенных реквизитов |
вложенных реквизитов |
|
|
|
1.1. Код вида модифицированного |
нормализованная строка символов. |
формируется с использованием порядкового |
1 |
|
|
высвобождения действующих веществ |
Шаблон: Ч){2} |
метода кодирования с шагом 1 |
|
|
|
1.2. Наименование вида |
нормализованная строка символов. |
формируется в виде словосочетания на русском |
1 |
|
|
модифицированного высвобождения |
Мин. длина: I. |
языке |
|
|
|
действующих веществ на русском |
Макс, длина: 500 |
|
|
|
|
языке |
|
|
|
|
|
1.3. Наименование вида |
нормализованная строка символов. |
формируется в виде словосочетания на |
0..1 |
|
|
модифицированного высвобождения |
Мин. длина: 1. |
английском языке |
|
|
|
действующих веществ на английском |
Макс, длина: 500 |
|
|
|
|
тыке |
|
|
|
|
|
1 |
.4. Определение вида |
нормализованная строка символов. |
формируется в виде текста на русском языке |
0..1 |
|
|
модифицированного высвобождения |
Мин. длина: 1. |
|
|
|
|
действующих веществ на русском |
Макс, длина: 4 ООО |
|
|
|
|
языке |
|
|
|
|
|
1.5. Сведения о записи справочника |
определяется областями значений |
определяются правилами формирования |
1 |
|
|
(классификатора) |
вложенных реквизитов |
вложенных реквизитов |
|
|
|
1.5.1. Дата начала действия |
обозначение даты в соответствии |
соответствует дате начала действия, указанной в |
1 |
|
|
|
с ГОСТ ИСО 8601-2001 в формате |
акте органа Евразийского зкономического союза |
|
|
|
|
YYYY-MM-DD |
|
|
|
|
Наименование реквизита |
Область значения реквизита |
Правила формирования значения реквизита |
Ми. |
|
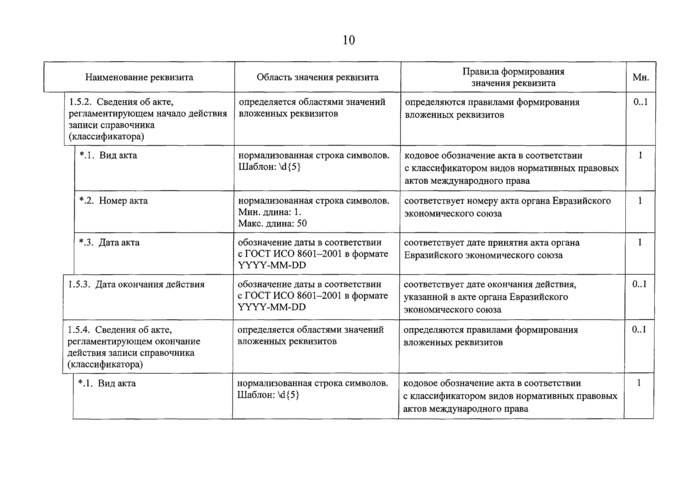
1.5.2. Сведения об акте.
pei ламе и тирующем начало действия
записи справочника
(классификатора) |
определяется областями значений вложенных реквизитов |
определяются правилами формирования вложенных реквизитов |
0..1 |
|
|
М. Вид акта |
нормализованная строха символов. Шаблон: d{5} |
кодовое обозначение акта в соответствии с классификатором видов нормативных правовых актов международного права |
1 |
|
•.2. Номер акта |
нормализованная строка символов. Мин. длина: 1.
Макс, длина: 50 |
соответствует номеру акта органа Евразийского экономического союза |
1 |
|
*.3. Дата акта |
обозначение даты в соответствии с ГОСТ ИСО 8601-2001 в формате YYYY-MM-DD |
соответствует дате принятия акта органа Евразийского экономического союза |
1 |
|
1.5.3. Дата окончания действия |
обозначение даты в соответствии с ГОСТ ИСО 8601-2001 в формате YYYY-MM-DD |
соответствует дате окончания действия, указанной в акте органа Евразийского экономического союза |
0..I |
|
1.5.4. Сведения об акте, регламентирующем окончание действия записи справочника (классификатора) |
определяется областями значений вложенных реквизитов |
определяются правилами формирования вложенных реквизитов |
0..I |
|
|
*.1. Вид акта |
нормализованная строка символов. Шаблон: Vd{5} |
кодовое обозначение акта в соответствии с классификатором видов нормативных правовых актов международного права |
1 |
|
Наименование реквизита |
Область значения реквизита |
Правила формирования значения реквизита |
Мн. |
|
|
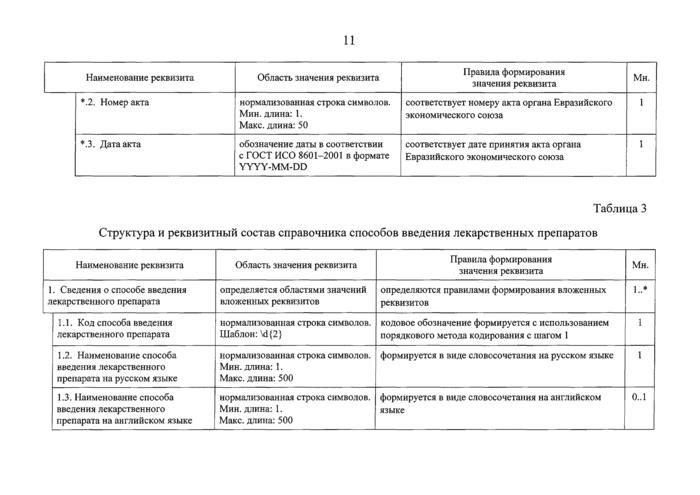
•.2. Номер акта |
нормализованная строка символов. Мин. длина: 1.
Макс, длина: 50 |
соответствует номеру акта органа Евразийского экономического союза |
1 |
|
|
♦.3. Дата акта |
обозначение даты в соответствии с ГОСТ ИСО «601-2001 в формате YYYY-MM-DD |
соответствует дате принятия акта органа Евразийского экономическою союза |
1 |
|
|
Таблица 3 |
|
Структура и реквизитный состав справочника способов введения лекарственных препаратов |
|
Наименование реквизита |
Область значения реквизита |
Правила формирования значения реквизита |
Мн. |
|
1 |
. Сведения о способе введения |
определяется областями значений |
определяются правилами формирования вложенных |
1..* |
|
лекарственного препарата |
вложенных реквизитов |
реквизитов |
|
|
|
1.1. Код способа введения |
нормализованная строка символов. |
кодовое обозначение формируется с использованием |
1 |
|
|
лекарственного препарата |
Шаблон: \d{2} |
порядкового метода кодирования с шагом 1 |
|
|
|
1.2. Наименование способа |
нормализованная строка символов. |
формируется в виде словссочетами* на русском языке |
1 |
|
|
введения лекарственного |
Мин. длина: 1. |
|
|
|
|
препарата на русском языке |
Макс, длина: 500 |
|
|
|
|
1.3. Наименование способа |
нормализованная строка символов. |
формируется в виде словосочетания на английском |
0..1 |
|
|
введения лекарственного |
Мин. длина: 1. |
языке |
|
|
|
препарата на английском языке |
Макс, длина: 500 |
|
|
|
|
Наименование реквизита |
Область значения реквизита |
Правила формирования значения реквизита |
Мн. |
|
|
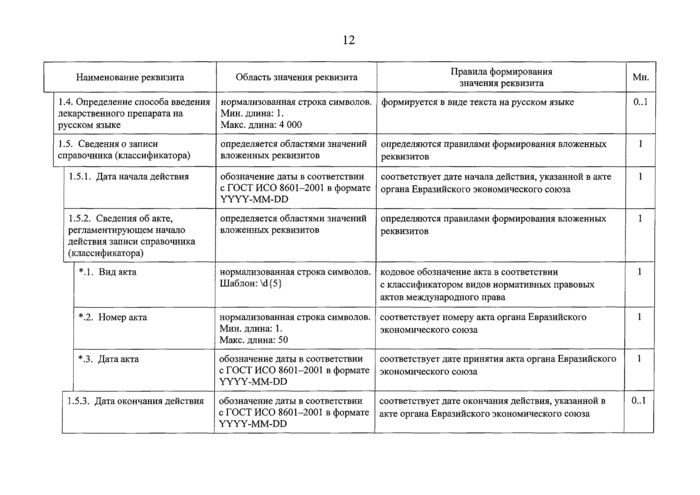
1.4. Определение способа введения лекарственного препарата на русском языке |
нормализованная строка символов. Мин. длина: 1.
Макс, длина: 4 ООО |
формируется в виде текста на русском языке |
0..1 |
|
1.5. Сведения о записи справочника (классификатора) |
определяется областями значений вложенных реквизитов |
определяются правилами формирования вложенных реквизитов |
1 |
|
|
|
1.5.1. Дата начала действия |
обозначение даты в соответствии с ГОСТ ИСО 8601-2001 в формате YYYY-MM-DD |
соответствует дате начала действия, указанной в акте органа Евразийского экономического союза |
1 |
|
|
1.5.2. Сведения об акте, регламентирующем начало действия записи справочника (классификатора) |
определяется областями значений вложенных реквизитов |
определяются правилами формирования вложенных реквизитов |
1 |
|
|
|
•Л. Вид акта |
нормализованная строка символов. Шаблон: М{5) |
кодовое обозначение акта в соответствии с классификатором видов нормативных правовых актов международного права |
1 |
|
|
*.2. Номер акта |
нормализованная строка символов. Мин. .длина: 1.
Макс, длина: 50 |
соответствует номеру акта органа Евразийского экономического союза |
1 |
|
|
|
•.3. Дата акта |
обозначение даты в соответствии с ГОСТ ИСО 8601-2001 н формате YYYY-MM-DD |
соответствует дате принятия акта органа Евразийского экономического союза |
1 |
|
|
1.5.3. Дата окончания действия |
обозначение даты в соответствии с ГОСТ ИСО 8601-2001 в формам YYYY-MM-DD |
соответствует дате окончания действия, указанной в акте органа Евразийского экономического союза |
0..1 |
|
Наименование реквизита |
Область значения реквизита |
11равила формирования значения реквизита |
Мн. |
|
|
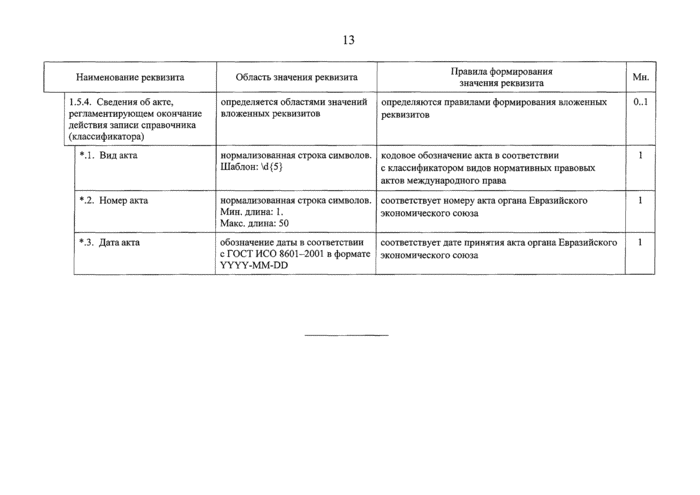
1.5.4. Сведения об акте, регламентирующем окончание действия записи справочника (классификатора) |
определяется областями значений вложенных реквизитов |
определяются правилами формирования вложенных реквизитов |
0..1 |
|
|
•Л. Вид акта |
нормализованная строка символов. Шаблон: \d{5} |
кодовое обозначение акта в соответствии с классификатором видов нормативных правовых актов международного права |
1 |
|
|
•.2. Номер акта |
нормализованная строка символов. Мин. длина: 1.
Макс, длина: 50 |
соответствует номеру акта органа Евразийского экономического союза |
1 |
|
|
♦.3. Дата акта |
обозначение даты в соответствии с ГОСТ ИСО 8601-2001 в формате YYYY-MM-DD |
соответствует дате принятия акта органа Евразийского экономического союза |
1 |
УТВЕРЖДЕН
Решением Коллегии Евразийской экономической комиссии от 17 сентября 2019 г. № 158
СПРАВОЧНИК путей введении лекарственных препаратов
I. Паспорт справочника
|
№
п/п |
Обозначение элемента |
Описание |
|
1 |
2 |
3 |
|
1 |
Код |
029 |
|
2 |
Тип |
1 - справочник |
|
3 |
Наименование |
справочник путей введения лекарственных препаратов |
|
4 |
Аббревиатура |
СПВЛП |
|
5 |
Обозначение |
ЕС 029-2019 (ред. 1) |
|
6 |
Реквизиты акта о принятии (утверждении) справочника (классификатора) |
Решение Коллегии Евразийской экономической комиссии от 17 сентября 2019 г. № 158 |
|
7 |
Дата введения в действие (начала применения) справочника (классификатора) |
19 октября 2019 г. |
|
8 |
Реквизиты акта о прекращении применения справочника (классификатора) |
' |
|
9 |
Дата окончания применения справочника (классификатора) |
- |
|
10 |
Оператор (операторы) |
BY, Министерство здравоохранения Республики Беларусь. Уполномоченная организация: Республиканское унитарное предприятие «Центр экспертиз и испытаний в здравоохранении » |
|
№
п/п |
Обозначение элемента |
Описание |
|
1 |
2 |
3 |
|
11 |
Назначение |
справочник предназначен для унификации наименований путей введения лекарственных препаратов, используемых при маркировке лекарственных препаратов, составлении регистрационного досье лекарственных препаратов, формировании единого реестра зарегистрированных лекарственных средств Евразийского экономического союза и информационных баз данных в сфере обращения лекарственных средств |
|
12 |
Аннотация (область применения) |
используется при формировании предоставляемых субъектами обращения лекарственных средств в уполномоченные органы государств - членов Евразийского экономического союза документов, в том числе в электронном виде, а также для обеспечения информационного взаимодействия при реализации общих процессов в рамках Евразийского экономического союза |
|
13 |
Ключевые слова |
лекарственная форма, путь введения |
|
14 |
Сфера, в которой реализуются полномочия органов Евразийского экономического союза |
техническое регулирование |
|
15 |
Использование международной (межгосударственной, региональной) классификации |
1 - справочник гармонизирован с международным (межгосударственным, региональным) стандартом ИСО 11239 «Информатизация здоровья. Идентификация лекарственных средств. Элементы данных и структуры для уникальной идентификации и обмена информацией о регистрируемых формах дозировки, единицах представления, путях введения и упаковке» |
|
16 |
Наличие государственных справочников (классификаторов) государств - членов Евразийского экономического союза |
2 - справочник не имеет аналогов в государствах - членах Евразийского экономического союза |
|
№
п/п |
Обозначение элемента |
Описание |
|
1 |
2 |
3 |
|
17 |
Метод систематизации (классификации) |
1 - порядковый метод систематизации |
|
18 |
Методика ведения |
справочник ведется в электронном виде в соответствии с Порядком ведения номенклатуры лекарственных форм и справочника путей введения лекарственных препаратов, утвержденным Решением Коллегии Евразийской экономической комиссии от 17 сентября 2019 г. № 158 |
|
19 |
Структура |
структура и реквизитный состав справочника (состав полей справочника, области их значений и правила формирования) приведены в разделе 11 настоящего справочника |
|
20 |
Степень конфиденциальности |
сведения из справочника относятся |
|
|
данных |
к информации открытого доступа |
|
21 |
Установленная периодичность пересмотра |
не установлена |
|
22 |
Изменения |
- |
|
23 |
Ссылка на детализированные |
детализированные сведения из справочника |
|
|
сведения из справочника |
приведены на информационном портале |
|
|
(классификатора) |
Евразийского экономического союза |
|
24 |
Способ представления |
опубликование на информационном портале |
|
|
сведений из справочника (классификатора) |
Евразийского экономического союза |
II. Описание структуры справочника
1. Настоящий раздел устанавливает требования к структуре справочника, в том числе определяет реквизитный состав и структуру справочника, области значений реквизитов и правила их формирования.
2. Структура и реквизитный состав справочника приведены в таблице, в которой формируются следующие поля (графы):
«область значения реквизита» - текст, поясняющий смысл (семантику) реквизита;
«правила формирования значения реквизита» - текст, уточняющий назначение реквизита, определяющий правила его формирования (заполнения), или словесное описание возможных значений реквизита;
«мн.» - множественность реквизита (обязательность
(опциональность) и количество возможных повторений реквизита).
3. Для указания множественности реквизитов передаваемых данных используются следующие обозначения:
1 - реквизит обязателен, повторения не допускаются;
п - реквизит обязателен, должен повторяться п раз (n > 1);
1..* - реквизит обязателен, может повторяться без ограничений;
п..* - реквизит обязателен, должен повторяться не менее п раз (n> 1);
п..ш - реквизит обязателен, должен повторяться не менее п раз и не более ш раз (n > 1, ш > п);
0..1 - реквизит опционален, повторения не допускаются;
0..* - реквизит опционален, может повторяться без ограничений;
0..ш - реквизит опционален, может повторяться не более ш раз
(ш> 1).
Таблица
|
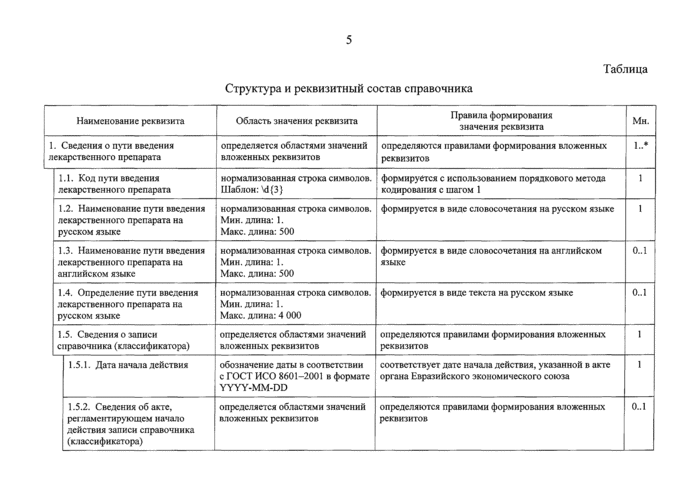
Структура и реквизитный состав справочника |
|
Наименование реквизита |
Область значения реквизита |
Правила формирования значения реквизита |
Мн. |
|
1. Сведения о пути введения |
определяется областями значений |
определяются правилами формирования вложенных |
1..* |
|
лекарственного препарата |
вложенных реквизитов |
реквизитов |
|
|
|
1.1. Код пути введения |
нормализованная строка символов. |
формируется с использованием порядкового метода |
1 |
|
|
лекарственного препарата |
Шаблон: <1{3} |
кодирования с шагом 1 |
|
|
|
1.2. Наименование пути введения |
нормализованная строка символов. |
формируется в виде словосочетания на русском языке |
1 |
|
|
лекарственного препарата на |
Мин. длина: 1. |
|
|
|
|
русском языке |
Макс, длина: 500 |
|
|
|
|
1.3. Наименование пути введения |
нормализованная строка символов. |
формируется в виде словосочетания на английском |
0..1 |
|
|
лекарственного препарата на |
Мин. длина: 1. |
языке |
|
|
|
английском языке |
Макс, длина: 500 |
|
|
|
|
1.4. Определение пути введения |
нормализованная строка символов. |
формируется в виде текста на русском языке |
0..1 |
|
|
лекарственного препарата на |
Мин. длина: 1. |
|
|
|
|
русском языке |
Макс, длина: 4 ООО |
|
|
|
|
1.5. Сведения о записи |
определяется областями значений |
определяются правилами формирования вложенных |
1 |
|
|
справочника (классификатора) |
вложенных реквизитов |
реквизитов |
|
|
|
1.5.1. Дата начала действия |
обозначение даты в соответствии |
соответствует дате начала действия, указанной в акте |
1 |
|
|
|
с ГОСТ ИСО 8601-2001 и формате |
органа Евразийского экономического союза |
|
|
|
|
YYYY-MM-DD |
|
|
|
|
1.5.2. Сведения об акте. |
определяется областями значений |
определяются правилами формирования вложенных |
0..1 |
|
|
регламентирующем начало |
вложенных реквизитов |
реквизитов |
|
|
|
действия записи справочника |
|
|
|
|
|
(классификатора) |
|
|
|
|
УТВЕРЖДЕНА
Решением Коллегии Евразийской экономической комиссии от 17 сентября 2019 г. № 158
НОМЕНКЛАТУРА лекарственных форм
|
I. Паспорт номенклатуры |
|
Х>
п/п |
Обозначение элемента |
Описание |
|
1 |
2 |
3 |
|
1 |
Кол |
057 |
|
2 |
Тип |
2 - классификатор |
|
3 |
Наименование |
номенклатура лекарственных форм |
|
4 |
Аббревиатура |
НЛФ |
|
5 |
Обозначение |
ЕК 057-2019 (ред. 1) |
|
6 |
Реквизиты акта о принятии (утверждении) справочника (классификатора) |
Решение Коллегии Евразийской экономической комиссии от 17 сентября 2019 г. Ха 158 |
|
7 |
Дата введения в действие (начала применения) справочника (классификатора) |
с даты вступления в силу Решения Коллегии Евразийской экономической комиссии от 17 сентября 2019 г. № 158 |
|
8 |
Реквизиты акта о прекращении применения справочника (классификатора) |
|
|
9 |
Дата окончания применения справочника (классификатора) |
- |
|
10 |
Оператор (операторы) |
RU, Министерство здравоохранения Российской Федерации. Уполномоченная организация: федеральное государственное бюджетное учреждение «Научный центр экспертизы средств медицинского применения» Министерства здравоохранения Российской Федерации |
|
|
Наименование реквизита |
Область значения реквизита |
11 равила формирования значения реквизита |
Ми. |
|
|
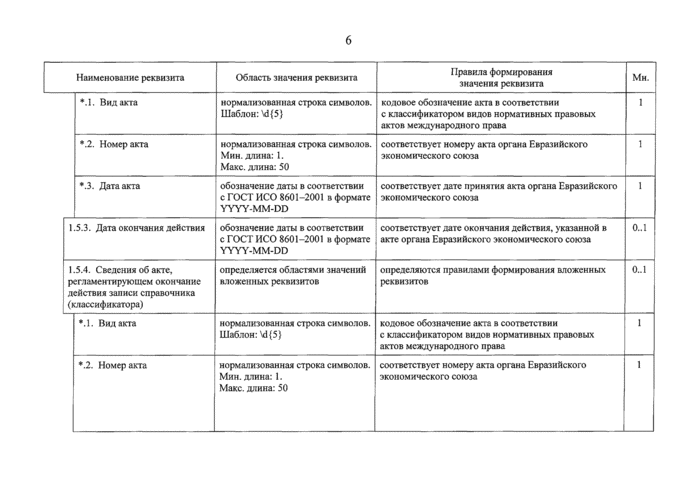
•Л. Вил акта |
нормализованная строка символов. Шаблон: d{5} |
кодовое обозначение акта в соответствии с классификатором видов нормативных правовых актов международного права |
1 |
|
|
•■2. Номер акта |
нормализованная строка символов. Мин. длина: 1.
Макс, длина: 50 |
соответствует номеру акта органа Евразийского экономического союза |
1 |
|
|
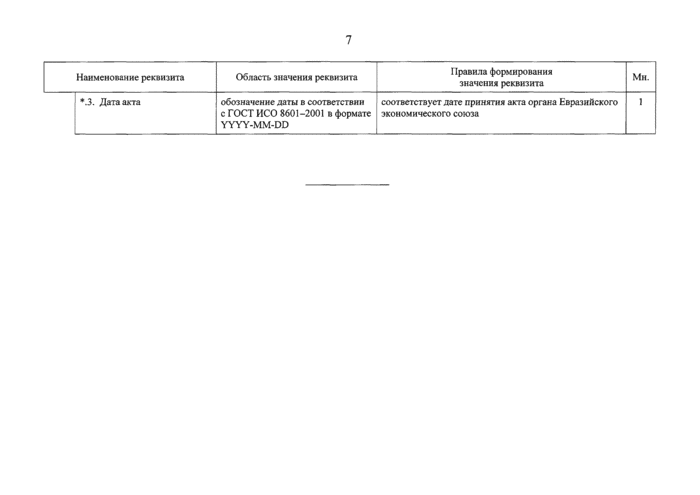
*.3. Дата акта |
обозначение даты в соответствии с ГОСТ ИСО 8601-2001 в формате YYYY-MM-DD |
соответствует дате принятия акта органа Евразийского экономического союза |
1 |
|
|
1.5.3. Дата окончания действия |
обозначение даты в соответствии с ГОСТ ИСО 8601-2001 и формате YYYY-MM-DD |
соответствует дате окончания действия, указанной в акте органа Евразийского экономического союза |
0..1 |
|
|
1.5.4. Сведения об акте, регламентирующем окончание действия записи справочника (классификатора) |
определяется областями значений вложенных реквизитов |
определяются правилами формирования вложенных реквизитов |
0..1 |
|
|
•Л. Вид акта |
нормализованная строка символов. Шаблон: Ч1{5 J |
кодовое обозначение акта в соответствии с классификатором видов нормативных правовых актов международного права |
1 |
|
|
•.2. Номер акта |
нормализованная строка символов. Мин. длина: 1.
Макс, хитина: 50 |
соответствует номеру акта органа Евразийского экономического союза |
1 |
|
№
п/п |
Обозначение элемента |
Описание |
|
1 |
2 |
3 |
|
11 |
Назначение |
классификатор предназначен для унификации наименований лекарственных форм, используемых при маркировке лекарственных препаратов, составлении регистрационного досье лекарственных препаратов, формировании единого реестра зарегистрированных лекарственных средств Евразийского экономического союза и информационных баз данных в сфере обращения лекарственных средств |
|
12 |
Аннотация (область применения) |
используется при формировании представляемых субъектами обращения лекарственных средств в уполномоченные органы государств - членов Евразийского экономического союза документов, в том числе в электронном виде, а также для обеспечения информационного взаимодействия при реализации общих процессов в рамках Евразийского экономического союза |
|
13 |
Ключевые слова |
лекарственная форма, лекарственный препарат, лекарственное средство, путь введения, способ введения, модификация высвобождения |
|
14 |
Сфера, в которой реализуются полномочия органов Евразийского экономического союза |
техническое регулирование |
|
15 |
Использование международной (межгосударственной, региональной) классификации |
1 - классификатор гармонизирован с международным (межгосударственным, региональным) стандартом ИСО 11239 «Информатизация здоровья. Идентификация лекарственных средств. Элементы данных и структуры для уникальной идентификации и обмена информацией о регистрируемых формах дозировки, единицах представления, путях введения и упаковке» |
|
№
п/п |
Обозначение элемента |
Описание |
|
1 |
2 |
3 |
|
16 |
Наличие государственных справочников (классификаторов) государств - членов Евразийского экономического союза |
2 - классификатор не имеет аналогов в государствах - членах Евразийского экономического союза |
|
17 |
Метод систематизации (классификации) |
4 - комбинированный метод классификации в соответствии с Методикой классификации и кодирования информации в номенклатуре лекарственных форм согласно приложению |
|
18 |
Методика ведения |
классификатор ведется в электронном виде в соответствии с Порядком ведения номенклатуры лекарственных форм и справочника путей введения лекарственных препаратов, утвержденным Решением Коллегии Евразийской экономической комиссии от 17 сентября 2019 г. № 158 |
|
19 |
Структура |
информация о структуре классификатора (состав полей классификатора, области их значений и правила формирования) приведена в разделе 11 настоящего документа |
|
20 |
Степень конфиденциальности данных |
сведения из классификатора относятся к информации открытого доступа |
|
21 |
Установленная периодичность пересмотра |
ежемесячно |
|
22 |
Изменения |
- |
|
23 |
Ссылка на детализированные сведения нз справочника (классификатора) |
детализированные сведения из классификатора приведены на информационном портале Евразийского экономического союза |
|
24 |
Способ представления сведений из справочника (классификатора) |
опубликование на информационном портале Евразийского экономического союза |
II. Описание структуры номенклатуры
1. Настоящий раздел устанавливает требования к структуре номенклатуры, в том числе определяет реквизитный состав и структуру номенклатуры, области значений реквизитов и правила их формирования.
2. Структура и реквизитный состав номенклатуры представляют собой совокупность структур и реквизитных составов номенклатуры лекарственных форм, справочника видов модифицированного высвобождения действующих веществ и справочника способов введения лекарственных препаратов, приведенных в таблицах 1 - 3, в которых формируются следующие поля (графы):
«область значения реквизита» - текст, поясняющий смысл (семантику) реквизита;
«правила формирования значения реквизита» - текст, уточняющий назначение реквизита, определяющий правила его формирования (заполнения), или словесное описание возможных значений реквизита;
«мн.» - множественность реквизита (обязательность
(опциональность) и количество возможных повторений реквизита).
3. Для указания множественности реквизитов передаваемых данных используются следующие обозначения:
1 - реквизит обязателен, повторения не допускаются;
п - реквизит обязателен, должен повторяться п раз (n > 1);
1..* - реквизит обязателен, может повторяться без ограничений;
п..* — реквизит обязателен, должен повторяться не менее п раз (n > 1);
п..ш - реквизит обязателен, должен повторяться не менее п раз и не более m раз (n > 1, ш > п);
0..1 - реквизит опционален, повторения не допускаются;
0. * - реквизит опционален, может повторяться без ограничений; 0..т - реквизит опционален, может повторяться не более m раз (m> 1).
|
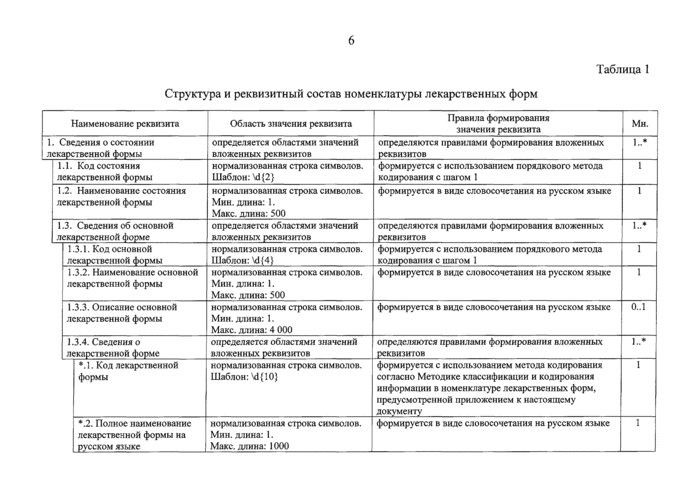
Таблица 1
Структура и реквизитный состав номенклатуры лекарственных форм |
|
Наименование реквизита |
Область значения реквизита |
Правила формирования значения реквизита |
Мн. |
|
1. Сведения о состоянии I лекарственной формы |
определяется областями значений вложенных реквизитов |
определяются правилами формирования вложенных реквизитов |
1 • |
|
|
1.1. Код состояния лекарственной формы |
нормализованная строка символов. Шаблон: \d{2} |
формируется с использованием порядкового метода кодирования с шагом 1 |
1 |
|
|
1.2. Наименование состояния лекарственной формы |
нормализованная строка символов. Мнн. длина: 1.
Макс, длина: 500 |
формируется в виде словосочетания на русском языке |
1 |
|
|
1.3. Сведения об основной лекарственной форме |
определяется областями значений вложенных реквизитов |
определяются правилами формирования аложеиных реквизитов |
1..* |
|
|
1.3.1. Код основной лекарственной формы |
нормализованная строка символов. Шаблон: ^{4) |
формируется с использованием порядкового метола кодирования с шагом 1 |
1 |
|
|
1.3.2. Наименование основной лекарственной формы |
нормализованная строка символов. Мин. длина: 1.
Макс, длина: 500 |
формируется в виде словосочетания на русском языке |
1 |
|
|
1.3.3. Описание основной лекарственной формы |
нормализованная строка символов. Мим. длина: 1.
Макс, длина: 4 ООО |
формируется в виде словосочетания на русском языке |
0..1 |
|
|
1.3.4. Сведения о лекарственной форме |
определяется областями значений вложенных реквизитов |
определяются правилами формирования вложенных реквизитов |
I..* |
|
|
|
•.1. Код лекарственной формы |
нормализованная строка символов. Шаблон: U {10} |
формируется с использованием метода кодирования согласно Методике классификации и кодирования информации в номенклатуре лекарственных форм, предусмотренной приложением к настоящему |
1 |
|
|
|
|
|
документу |
|
|
|
|
•.2. Полное наименование лекарственной формы на русском языке |
нормализованная строка символов. Мни. .пика- 1.
Макс, длина: 1000 |
формируется в виде словосочетания на русском языке |
1 |
|
|
Наименование реквизита |
Область значения реквизита |
Правила формирования значения реквизита |
Ми. |
|
|
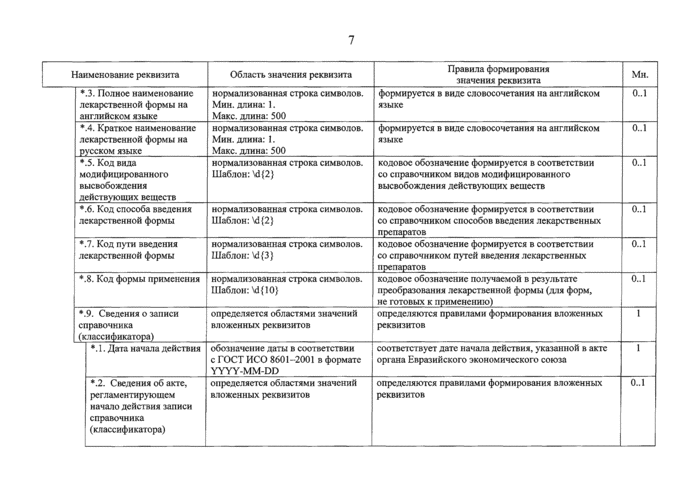
•.3. Полное наименование лекарственной формы на английском языке |
нормализованная строка символов. Мин. длина: 1.
Макс, длина: 500 |
формируется в виде словосочетания на английском языке |
0..1 |
|
•.4. Краткое наименование лекарственной формы на русском языке |
нормализованная строка символов. Мим. длима: 1.
Макс, длина: 500 |
формируется в виде словосочетания на английском языке |
0..1 |
|
*.5. Код вида модифицированного высвобождения действующих веществ |
нормализованная строка символов. Шаблон: -d{2> |
кодовое обозначение формируется в соответствии со справочником видов модифицированного высвобождения действующих веществ |
0..1 |
|
•.6. Код способа введения лекарственной формы |
нормализованная строка символов. Шаблон: ^{2} |
кодовое обозначение формируется в соответствии со справочником способов введения лекарственных препаратов |
0..1 |
|
•.7. Код пути введения лекарственной формы |
нормализованная строка символов. Шаблон: ^{3) |
кодовое обозначение формируется в соответствии со справочником путей введения лекарственных препаратов |
0..1 |
|
♦.8. Код формы применения |
нормализованная строка символов. Шаблон: \d{ 10) |
кодовое обозначение получаемой в результате преобразования лекарственной формы (для форм, нс готовых к применению) |
0..1 |
|
*.9. Сведения о записи
справочника
(классификатора) |
определяется областями значений вложенных реквизитов |
определяются правилами формирования вложенных реквизтпов |
1 |
|
|
|
". 1. Дата начала действия |
обозначение даты в соответствии с ГОСТ ИСО 8601- 2001 в формате YYYY-MM-DD |
соответствует дате начала действия, указанной в акте органа Евразийского экономического союза |
1 |
|
|
*.2. Сведения об акте, регламентирующем начало действия записи справочника (классификатора) |
определяется областями значений вложенных реквизитов |
определяются правилами формирования вложенных реквизитов |
0..1 |
|
Наименование реквизита |
Область значения реквизита |
Правила формирования значения реквизита |
Мн. |
|
|
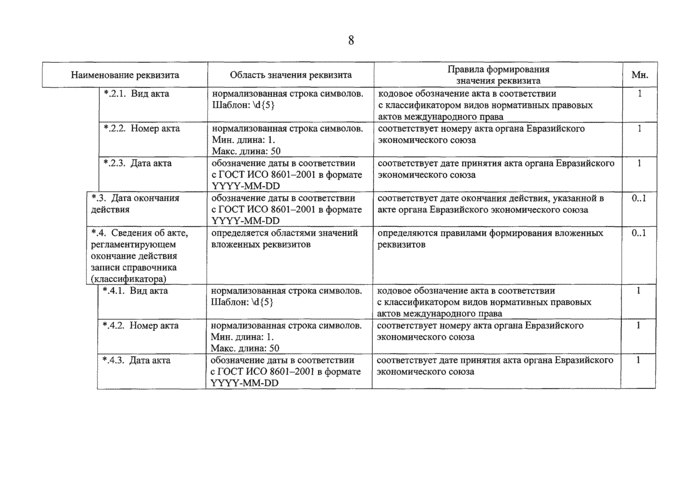
•21. Вид акта |
нормализованная строка символов. Шаблон: U{5} |
кодовое обозначение акта в соответствии с классификатором видов нормативных правовых актов международного права |
1 |
|
*.2.2. Номер акта |
нормализованная строка символов. Мин. длина: 1.
Макс, длина: 50 |
соответствует номеру акта органа Евразийского экономического союза |
1 |
|
|
|
•.2.3. Дата акта |
обозначение даты в соответствии с ГОСТ ИСО 8601-2001 в формате YYYY-MM-DD |
соответствует дате принятия акта органа Евразийского экономического союза |
1 |
|
|
•.3. Лага окончания действия |
обозначение даты в соответствии с ГОСТ ИСО 8601-2001 в формате YYYY-MM-DD |
соответствует дате окончания действия, указанной в акте органа Евразийского экономического союза |
0..1 |
|
•.4. Сведения об акте, регламентирующем окончание действия записи справочника (классификатора) |
определяется областями значений вложенных реквизитов |
определяются правилами формирования вложенных реквизитов |
0..1 |
|
|
|
*.4.1. Вид акта |
нормализованная строка символов. Шаблон: Vl{5} |
кодовое обозначение акта в соответствии с классификатором видов нормативных правовых актов международного нрава |
I |
|
|
•.4.2. Номерокта |
нормализованная строка символов. Мин. длина: 1.
Макс, длина: 50 |
соответствует номеру акта органа Евразийского экономического союза |
1 |
|
•.4.3. Лата акта |
обозначение даты в соответствии с ГОСТ ИСО 8601-2001 в формате YYYY-MM-DD |
соответствует дате принятия акта ораана Евразийского экономического союза |
1 |