Федеральная служба по
гидрометеорологии и мониторингу
окружающей среды (Росгидромет)
|
РУКОВОДЯЩИЙ
ДОКУМЕНТ
|
РД
52.24.504-2010
|
МАССОВАЯ КОНЦЕНТРАЦИЯ ЖИРОВ В ВОДАХ.
МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ
ИК-ФОТОМЕТРИЧЕСКИМ МЕТОДОМ
Ростов-на-Дону
2010
Предисловие
1 РАЗРАБОТАН Государственным учреждением Гидрохимический институт (ГУ
ГХИ)
2 РАЗРАБОТЧИКИ А.Г. Страдомская, д-р хим. наук, И.А. Рязанцева
3 СОГЛАСОВАН с НПО «Тайфун» 28.01.2010 и УМЗА Росгидромета 04.03.2010
4 УТВЕРЖДЕН Заместителем Руководителя Росгидромета 04.03.2010
5 АТТЕСТОВАН ГУ ГХИ, свидетельство об аттестации № 159.24-2009 от
05.06.2009
6 ЗАРЕГИСТРИРОВАН ЦМТР ГУ «НПО «Тайфун» 24.03.2010 за
номером РД 52.24.504-2010
7 ВЗАМЕН РД
52.24.504-98 «Методические указания. Методика выполнения измерений массовой
концентрации жиров в водах ИК - фотометрическим методом
СОДЕРЖАНИЕ
|
1 Область применения. 3
2 Нормативные ссылки. 3
3 Приписанные характеристики
погрешности измерения. 3
4 Средства измерений,
вспомогательные устройства, реактивы, материалы.. 4
4.1 Средства измерений, вспомогательные устройства. 4
4.2 Реактивы и материалы.. 5
5 Метод измерений. 6
6 Требования безопасности, охраны
окружающей среды.. 6
7 Требования к квалификации
операторов. 6
8 Условия выполнения измерений. 6
9 Отбор и хранение проб. 6
10 Подготовка к выполнению
измерений. 7
10.1 Приготовление растворов и реактивов. 7
10.2 Подготовка посуды для определения жиров. 8
10.3 Подготовка хроматографической пластинки. 8
10.4 Подготовка подвижной фазы.. 8
10.5 Подготовка проявляющей камеры с йодом.. 8
10.6 Подготовка приборов. 8
10.7 Приготовление градуировочного раствора. 8
10.8 Установление градуировочных зависимостей. 9
10.9 Контроль стабильности градуировочной
характеристики. 9
11 Выполнение измерений. 10
11.1 Холостое измерение. 10
11.2 Экстракция. 10
11.3 Выделение жиров методом тонкослойной хроматографии. 10
11.3 Измерение. 11
11.4 Мешающие влияния. 11
12 Вычисление и оформление
результатов измерений. 11
13 Контроль качества результатов
измерений при реализации методики в лаборатории. 12
13.1 Общие положения. 12
13.2 Алгоритм оперативного контроля процедуры
выполнения измерений с использованием метода добавок. 12
14 Проверка приемлемости
результатов, полученных в условиях воспроизводимости. 13
Приложение А. Методика приготовления аттестованного раствора жиров
АР-Ж... 13
|
Введение
В водные объекты жиры
поступают с хозяйственно-бытовыми сточными водами и сточными водами предприятий
мясомолочной, консервной, рыбообрабатывающей, кожевенной промышленности, боен,
жироперерабатывающих, шерстепрядильных фабрик, предприятий выпускающих
растительные масла, жирные кислоты, глицерин, мыла, жирозаменители и т.д.
Значительное количество жиров образуется в процессе фотосинтеза, метаболизма растительных
и животных организмов, их посмертном разложении. Жиры находятся в поверхностных
водах в растворенном, эмульгированном и сорбированном взвешенными веществами и
донными отложениями состояниях.
Жиры, в основном, состоят из
триглицеридов - полных сложных эфиров глицерина и жирных кислот. В состав
природных жиров входят жирные кислоты, содержащие четное число углерода. В
состав их также входят моно- и диглицериды, фосфолипиды, свободные жирные
кислоты, стеарины и их эфиры и т.д. Жирнокислотный состав животных жиров
представлен, в основном, олеиновой, линолевой, пальмитиновой и стеариновой
кислотами. Около 75 % растительных жиров (масел) составляют глицериды трех
кислот - пальмитиновой, олеиновой и линолевой. Большинство масел содержит 4 - 7
главных и несколько сопутствующих (менее 5 % от суммы) жирных кислот. Жиры
некоторых растений содержат специфические, характерные только для них, жирные
кислоты. Триглицериды могут быть однокислотными и разнокислотными (смешанными).
Однокислотные жиры (оливковое, касторовое масла) встречаются редко, подавляющее
большинство жиров представляет собой смеси разнокислотных триглицеридов.
Концентрации жиров в
природных водах могут колебаться от тысячных долей до миллиграммов в кубическом
дециметре воды.
Попадая в водные объекты в
повышенных концентрациях, жиры заметно ухудшают его кислородный режим, что
негативно влияет на их экологическое состояние.
Содержание жиров в природных
водах не нормируется.
РУКОВОДЯЩИЙ ДОКУМЕНТ
МАССОВАЯ КОНЦЕНТРАЦИЯ ЖИРОВ В ВОДАХ.
МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ
ИК-ФОТОМЕТРИЧЕСКИМ МЕТОДОМ
Дата введения 2010-04-06
1 Область применения
1.1 Настоящий руководящий
документ устанавливает методику выполнения измерений (далее - методика)
массовой концентрации жиров в природных и очищенных сточных водах в диапазоне
от 0,10 - 0,60 мг/дм3 ИК-фотометрическим методом.
При анализе проб воды с
массовой концентрацией жиров, превышающей 0,60 мг/дм3, допускается
выполнение измерений после разбавления элюата четыреххлористым углеродом, таким
образом, чтобы массовая концентрация жиров в разбавленном элюате находилась в
диапазоне от 0,040 до 0,060 мг/см3.
1.2 Настоящий руководящий
документ предназначен для использования в лабораториях, осуществляющих анализ
природных и очищенных сточных вод.
2 Нормативные ссылки
В настоящем руководящем
документе использованы ссылки на следующие нормативные документы:
ГОСТ
12.1.005-88 ССБТ. Общие санитарно-гигиенические требования к воздуху
рабочей зоны
ГОСТ
12.1.007-76 ССБТ. Вредные вещества. Классификация и общие требования безопасности
ГОСТ
17.1.5.04-81 Охрана природы. Гидросфера. Приборы и устройства для отбора,
первичной обработки и хранения проб природных вод. Общие технические условия
ГОСТ
17.1.5.05-85 Охрана природы. Гидросфера. Общие требования к отбору проб
поверхностных и морских вод, льда и атмосферных осадков
ГОСТ
Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и
результатов измерений. Часть 6. Использование значений точности на практике
ГОСТ Р 51592-2000 Вода. Общие
требования к отбору проб
МИ
2881-2004 Рекомендация. ГСИ. Методики количественного химического анализа.
Процедуры проверки приемлемости результатов анализа.
Примечание -
Ссылки на остальные нормативные документы приведены в разделах 4, А.3, А.4.
3 Приписанные характеристики
погрешности измерения
3.1 При соблюдении всех
регламентируемых методикой условий проведения измерений характеристики погрешности
результата измерения с вероятностью 0,95 не должны превышать значений,
приведенных в таблице 1.
Таблица 1 - Диапазон измерений, значения характеристик погрешности
и ее составляющих при принятой вероятности Р = 0,95
|
Диапазон измерений массовой
концентрации жиров, X, мг/дм3
|
Показатель повторяемости (среднеквадратическое
отклонение повторяемости) sr,
мг/дм3
|
Показатель воспроизводимости (среднеквадратическое
отклонение воспроизводимости) sR, мг/дм3
|
Показатель правильности (границы систематической
погрешности) ±Dc,
мг/дм3
|
Показатель точности (границы погрешности) ±D,
мг/дм3
|
|
От 0,10 до 0,40 включ.
|
0,16×Х
|
0,24×Х
|
0,06
|
0,05 + 0,38×Х
|
|
Св. 0,40 до 0,60 включ.
|
0,16×Х
|
0,24×Х
|
0,10
|
0,05 + 0,38×Х
|
3.2 Значения
показателя точности методики используют при:
- оформлении результатов
измерений, выдаваемых лабораторией;
- оценке деятельности
лаборатории на качество проведения измерений;
- оценке возможности
использования результатов измерений при реализации методики в конкретной
лаборатории.
4 Средства измерений,
вспомогательные устройства, реактивы, материалы
4.1 Средства измерений, вспомогательные устройства
4.1.1 ИК-спектрофотометр или ИК-фотометр,
обеспечивающий измерения при длине волны 3,42 мкм в кюветах с толщиной
поглощающего слоя не менее 40 мм (спектрофотометр ИК-40 или фотометр, входящий
в комплект анализаторов АН-2, КН-2, или аналогичный по характеристикам прибор).
4.1.2 Весы лабораторные высокого (II)
класса точности по ГОСТ 24104-2001.
4.1.3 Колбы мерные 2-го класса точности исполнения 2
по ГОСТ
1770-74 вместимостью 50 см3 - 7 шт.
4.1.4 Пипетки градуированные 2-го класса точности
исполнения 1, 2 по ГОСТ
29227-91 вместимостью: 1 см3 - 2 шт., 2 см3 - 1 шт.,
5 см3 - 2 шт.
4.1.5 Пипетка с одной отметкой 2-го класса точности
исполнения 2 по ГОСТ 29169-91
вместимостью 5 см3 - 1 шт.
4.1.6 Цилиндры мерные исполнения 1, 3 по ГОСТ
1770-74 вместимостью: 25 см3 - 2 шт., 50 см3 - 1 шт.,
500 см3 - 1 шт., 1000 см3 - 1 шт.
4.1.7 Цилиндр мерный исполнения 2 по ГОСТ
1770-74 с притертой пробкой вместимостью 50 см3 - 1 шт.
4.1.8 Пробирки градуированные исполнения 2, с
взаимозаменяемым конусом 14/23, по ГОСТ
1770-74 с притертыми стеклянными пробками вместимостью 10 см3 -
10 шт.
4.1.9 Колбы типа Кн исполнения 1 со взаимозаменяемым
конусом 14/23, ТХС, по ГОСТ
25336-82 с притертыми стеклянными пробками вместимостью 50 см3 -
6 шт.
4.1.10 Колбы типа Кн исполнения 1 со взаимозаменяемым
конусом 29/32, ТХС, по ГОСТ
25336-82 с притертыми стеклянными пробками вместимостью 100 см3
- 2 шт.; 500 см3 - 1 шт.
4.1.11 Стаканы В-1 или В-2, ТХС, по ГОСТ
25336-82 вместимостью 5 - 10 см3 - 6 шт.
4.1.12 Стаканы В-1, ТХС, по ГОСТ
25336-82 вместимостью: 50 см3 - 1 шт., 600 см3 - 1
шт., 1000 см3 - 1 шт.
4.1.13 Стаканчики для взвешивания (бюксы) СВ-19/9 и
24/10 по ГОСТ
25336-82 - 2 шт.
4.1.14 Воронки делительные ВД исполнения 1, 3, ХС, по ГОСТ
25336-82 вместимостью 1000 см3 - 4 шт.
4.1.15 Воронки лабораторные, тип В по ГОСТ
25336-82 диаметром 36 мм - 6 шт.
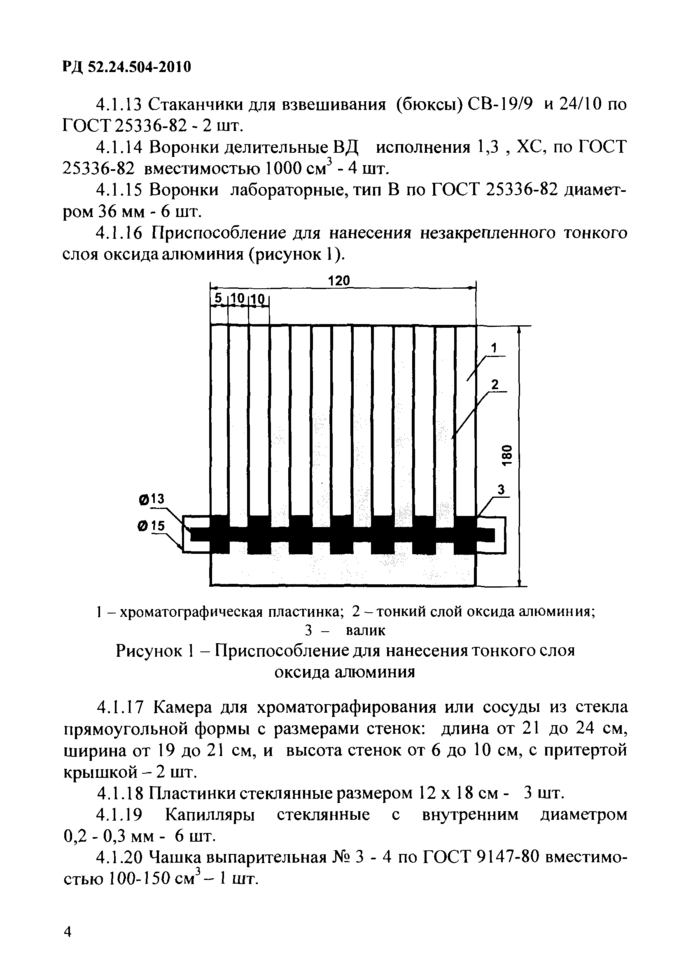
4.1.16 Приспособление для нанесения незакрепленного
тонкого слоя оксида алюминия (рисунок 1).
1 - хроматографическая пластинка; 2
- тонкий слой оксида алюминия; 3 - валик
Рисунок 1 - Приспособление для нанесения
тонкого слоя оксида алюминия
4.1.17 Камера для
хроматографирования или сосуды из стекла прямоугольной формы с размерами
стенок: длина от 21 до 24 см, ширина от 19 до 21 см, и высота стенок от 6 до 10
см, с притертой крышкой - 2 шт.
4.1.18 Пластинки стеклянные размером 12´18 см - 3 шт.
4.1.19 Капилляры стеклянные с внутренним диаметром 0,2
- 0,3 мм - 6 шт.
4.1.20 Чашка выпарительная № 3 - 4 по ГОСТ
9147-80 вместимостью 100 - 150 см3 - 1 шт.
4.1.21 Установка из стекла для перегонки
растворителей, включающая перегонную колбу вместимостью 1000 см3 с
взаимозаменяемым конусом 29/32; ёлочный дефлегматор длиной не менее 25 см с
взаимозаменяемыми конусами 14/23, 29/32; насадка типа Н1 с взаимозаменяемыми
конусами 14/23; холодильник ХПТ длиной не менее 30 см с взаимозаменяемым
конусом 14/23; аллонж по ГОСТ
25336-82, термометр ртутный с диапазоном от 0 до 100 °С по ГОСТ
13646-68.
4.1.22 Эксикаторы исполнения 2, диаметром корпуса 190
- 250 мм по ГОСТ
25336-82 - 2 шт.
4.1.23 Палочки стеклянные - по ГОСТ
27460-87 - 6 шт.
4.1.24 Флаконы стеклянные с притертыми пробками для
хранения экстрактов вместимостью 50 см3.
4.1.25 Посуда стеклянная с притертыми или корковыми
или пластиковыми пробками, обернутыми алюминиевой фольгой и двойным слоем
тефлоновой пленки для хранения проб вместимостью 0,5 - 1,0 дм3.
4.1.26 Склянки темного стекла для хранения
растворителей вместимостью 1 дм3.
4.1.27 Сито с диаметром отверстий 0,1 мм.
4.1.28 Скальпель.
4.1.29 Шпатель по ГОСТ
9147-80.
4.1.30 Штатив для пробирок.
4.1.31 Штатив для делительных воронок.
4.1.32 Холодильник бытовой.
4.1.33 Печь муфельная по ТУ 79 РСФСР 337-82.
4.1.34 Электроплитка с закрытой спиралью по ГОСТ
14919-83.
4.1.35 Шкаф сушильный общелабораторного назначения.
Примечание -
Допускается использование других типов средств измерений, посуды и
вспомогательного оборудования, в том числе импортных, с характеристиками не
хуже, чем у приведенных в 4.1.
4.2 Реактивы и материалы
4.2.1 Тристеарин по ТУ
6-09-07-926-77, ч.
4.2.2 Углерод
четыреххлористый по ГОСТ 20288-74,
х.ч., или ТУ 6-09-3219-84, ос.ч.
4.2.3 Хлороформ
(трихлорметан) по ГОСТ
20015-88, очищенный.
4.2.4 н-Гексан по ТУ
6-09-06-657-75, х.ч.
4.2.5 Ацетон по ТУ
2633-039-44493179-00, ос.ч.
4.2.6 Натрий сернокислый,
безводный (натрия сульфат) по ГОСТ 4166-76, ч.
4.2.7 Оксид алюминия для
хроматографии по ТУ 6-09-3916-75 или оксид алюминия активный по ГОСТ
8136-85, ч.д.а.
4.2.8 Кислота уксусная,
ледяная по ГОСТ
61-75, ч.д.а.
4.2.9 Кислота серная по ГОСТ 4204-77.
4.2.10 Йод по ГОСТ 4159-79, ч.д.а.
4.2.11 Кальций хлорид обезвоженный
по ТУ 6-09-4711-81, ч. (для эксикатора).
4.2.12 Вода дистиллированная
по ГОСТ
6709-72.
4.2.13 Фильтры бумажные
обеззоленные «белая лента» по ТУ 6-09-1678-86, диаметром не более 6 см.
Примечание -
Допускается использование реактивов, изготовленных по другой нормативной и
технической документации, в том числе импортных, с квалификацией не ниже
указанной в 4.2.
5 Метод измерений
Выполнение измерений основано
на выделении жиров из воды двукратной экстракцией хлороформом, концентрировании
и хроматографическом разделении экстракта в тонком слое оксида алюминия в
системе подвижных растворителей гексан - четыреххлористый углерод - ледяная
уксусная кислота. Жиры элюируют из соответствующей зоны оксида алюминия на
пластинке четыреххлористым углеродом и в элюатах количественно определяют жиры
по интенсивности поглощения С-Н связей метиленовых (-СН2-) и
метильных (-СН3-) групп в инфракрасной области спектра (l = 2926 см-1 или 3,42 мкм).
6 Требования безопасности,
охраны окружающей среды
6.1 При выполнении измерений
массовой концентрации жиров в пробах природных и очищенных сточных вод
соблюдают требования безопасности, установленные в национальных стандартах и
соответствующих нормативных документах.
6.2 По степени воздействия на
организм вредные вещества, используемые при выполнении измерений, относятся ко
2-му, 3-му и 4-му классам опасности по ГОСТ
12.1.007.
6.3 Содержание используемых
вредных веществ в воздухе рабочей зоны не должно превышать установленных
предельно допустимых концентраций в соответствии с ГОСТ
12.1.005.
6.4 Вредно действующие
вещества подлежат сбору и утилизации в соответствии с установленными правилами.
6.5 Дополнительных требований
по экологической безопасности не предъявляется.
7 Требования к квалификации
операторов
К выполнению измерений
допускаются лица со средним профессиональным образованием, имеющие стаж работы
в лаборатории не менее года и освоившие методику.
8 Условия выполнения измерений
При выполнении измерений в
лаборатории должны быть соблюдены следующие условия:
- температура окружающего
воздуха (22 ± 5) °С;
- атмосферное давление от
84,0 до 106,7 кПа (от 630 до 800 мм рт. ст.);
- влажность воздуха не более
80 % при 25 °С;
- напряжение в сети (220 ±
10) В;
- частота переменного тока в
сети питания (50 ± 1) Гц.
9 Отбор и хранение проб
Отбор проб для выполнения
измерений массовой концентрации жиров производится в соответствии с ГОСТ
17.1.5.05 и ГОСТ
Р 51592. Оборудование для отбора проб должно соответствовать ГОСТ
17.1.5.04 и ГОСТ
Р 51592. При отборе должен быть исключен захват поверхностной пленки воды.
Отобранные пробы, не фильтруя, помещают в стеклянную посуду, которая
закрывается притертыми стеклянными или корковыми или пластиковыми (не
резиновыми!) пробками, обернутыми алюминиевой фольгой и двойным слоем тонкой
тефлоновой пленки. Пробу для определения жиров помещают в отдельную посуду и
используют целиком. Объем отобранной пробы зависит от концентрации жиров в воде
и должен составлять не менее 0,5 дм3 для проб очищенных сточных вод
и не менее 1 дм3 для проб природных вод.
Экстракция пробы должна быть
выполнена в течение 1 сут. после отбора. Если это невозможно, пробы
консервируют, добавляя 5 см3 четыреххлористого углерода или
хлороформа на 1 дм3 воды. Хранят законсервированные пробы в
холодильнике две недели, экстракты в плотно закрытой посуде - до 2 месяцев.
10 Подготовка к выполнению
измерений
10.1
Приготовление растворов и реактивов
10.1.1 Оксид алюминия
Оксид алюминия просеивают
через сито и используют фракцию, прошедшую через сито (менее 0,1 мм). Хранят в
колбе с притертой пробкой, помещенной в эксикатор в течение месяца.
10.1.2 Углерод
четыреххлористый
Проверяют чистоту каждой
партии четыреххлористого углерода, выполняя измерение концентрации соединений,
поглощающих в ИК-области, используя для сравнения очищенный четыреххлористый
углерод. Если концентрация этих соединений превышает 0,01 мг/см3,
выполняют очистку четыреххлористого углерода следующим образом.
В делительную воронку
вместимостью 1000 см3 помещают 400 см3 четыреххлористого
углерода, добавляют 500 см3 дистиллированной воды и встряхивают в
течение 3 мин. Слой четыреххлористого углерода сливают в колбу. Процедуру
повторяют с новой порцией дистиллированной воды.
К промытому четыреххлористому
углероду добавляют около 10 г безводного сульфата натрия, встряхивают и
оставляют на 10 мин. Обезвоженный четыреххлористый углерод декантируют в
перегонную колбу и перегоняют, отбирая фракцию с температурой кипения от 76,7
°С до 76,8 °С. Хранят в склянке из темного стекла с притертой пробкой до
повышения значения холостого опыта.
10.1.3 Хлороформ
Проверяют чистоту каждой
партии хлороформа, для чего 25 см3 хлороформа помешают в стакан
вместимостью 50 см3 и оставляют в вытяжном шкафу при комнатной
температуре для упаривания. После уменьшения объема хлороформа примерно до 2 см3
переносят его в стаканчик вместимостью 5 - 10 см3, ополаскивая
стакан 0,5 см3 хлороформа, и оставляют до полного упаривания.
Остаток после упаривания растворяют в 10 см3 четыреххлористого
углерода и измеряют концентрацию соединений, поглощающих в ИК-области. Если
концентрация этих соединений превышает 0,01 мг/см3, выполняют
очистку хлороформа перегонкой, отбирая фракцию с температурой кипения 61,2 °С.
Хранят хлороформ в склянке из темного стекла и в темном месте.
10.1.5
Сульфат натрия (безводный)
Для удаления органических
примесей сульфат натрия прокаливают при 400 °С в течение 8 ч. Хранят в
эксикаторе 1 мес.
10.1.6
Тристеарин
Тристеарин очищают методом тонкослойной хроматографии.
Для этого растворяют 80 - 100 мг тристеарина в 0,3 - 0,4 см3
четыреххлористого углерода или хлороформа и с помощью капилляра малыми порциями
(0,01 - 0,02 см3) наносят на 4 сплошные хроматографические пластинки
с оксидом алюминия на расстоянии 6 - 7 мм от края в виде рядом расположенных
небольших пятен, образующих сплошные полосы шириной не более 2 мм.
После испарения растворителя помещают пластинки в
хроматографическую камеру (см. 11.3)
под углом 20° - 30°. Когда фронт подвижной фазы достигнет верхнего края оксида
алюминия, пластинку вынимают и, после испарения растворителя (через 5 - 10
мин), помещают в проявляющую камеру, предварительно насыщенную парами йода.
Зону тристеарина, обнаруженную в виде коричневой полосы на пластинках при
проявлении в парах йода (Rf = 0,45 - 0,55), после испарения последнего переносят
в воронку с фильтром и элюируют тристеарин с оксида алюминия 20 - 25 см3
четыреххлористого углерода, добавляя его небольшими порциями (не более 3 см3)
в бюкс. Растворитель удаляют под тягой до получения постоянного значения массы
бюкса с препаратом. Очищенный таким образом тристеарин используют для
приготовления градуировочного раствора. Массовая доля основного вещества в
полученном препарате не менее 98 %.
10.1.7 Дистиллированная вода,
очищенная четыреххлористым углеродом
Дистиллированную воду
экстрагируют в делительной воронке четыреххлористым углеродом из расчета 20 см3
растворителя на 1 дм3 воды. После расслоения фаз четыреххлористый
углерод отбрасывают в специальную емкость для слива, а дистиллированную воду
выливают в чистую склянку. Используется только свежеочищенная дистиллированная
вода.
10.2
Подготовка посуды для определения жиров
Посуду, используемую для приготовления растворов и
выполнения измерений массовой концентрации жиров в пробах воды, промывают
концентрированной серной кислотой, затем отмывают водопроводной водой и
ополаскивают дистиллированной водой. Кислоту используют многократно.
Для проверки чистоты посуды на присутствие примесей
поглощающих в ИК-области ее ополаскивают небольшими объемами четыреххлористого
углерода (от 5 до 10 см3 в зависимости от размера посуды) и измеряют
ИК-поглощение смыва. Концентрация поглощающих в ИК-области примесей при этом
должна быть менее 0,01 мг/см3.
10.3 Подготовка
хроматографической пластинки
На чисто вымытую стеклянную
пластинку насыпают немного оксида алюминия и с помощью специального
приспособления - валика (см. рисунок 1),
наносят 6 полос шириной 10 мм. Толщина слоя оксида алюминия должна составлять 1
мм.
Избыток оксида алюминия между
полосами и по краям пластинки счищают скальпелем.
10.4
Подготовка подвижной фазы
В мерный цилиндр с притертой пробкой вместимостью 50
см3 добавляют 35 см3 гексана, 15 см3
четыреххлористого углерода, 1 см3 ледяной уксусной кислоты и
перемешивают. Смесь готовят перед использованием.
10.5 Подготовка
проявляющей камеры с йодом
В камеру (см. 4.1.17) помещают 1 - 2 г
мелкокристаллического йода, распределив его равномерно по дну камеры, и
оставляют не менее чем на 30 мин. для насыщения ее парами йода.
10.6 Подготовка приборов
Включение, вывод на режим и
настройку ИК-фотометра осуществляют в соответствии с руководством по его
эксплуатации.
10.7 Приготовление
градуировочного раствора
10.7.1 Градуировочный
(аттестованный) раствор АР-Ж с массовой концентрацией тристеарина 1,00 мг/см3
готовят из очищенного тристеарина в соответствии с приложением А.
Раствор хранят в плотно
закрытой склянке из темного стекла в холодильнике не более 3 мес.
10.7.2 При отсутствии
тристеарина допускается использовать бараний жир, по составу наиболее близкий к
тристеарину. Очистка бараньего жира и приготовление аттестованного раствора
выполняются аналогично очистке и приготовлению аттестованного раствора из
тристеарина (см. 10.1.5 и
приложение А).
10.8
Установление градуировочных зависимостей
Для приготовления градуировочных образцов
градуированными пипетками вместимостью 1 см3 и 5 см3
вносят 0,50; 1,0; 1,5; 2,0; 3,0 см3 градуировочного раствора с
массовой концентрацией тристеарина 1,00 мг/см3 в мерные колбы
вместимостью 50 см3. Доводят объём в колбах до метки
четыреххлористым углеродом и тщательно перемешивают. Массовые концентрации
тристеарина в полученных градуировочных образцах равны, соответственно, 0,010;
0,020; 0,030; 0,040; 0,060 мг/см3.
Установление градуировочной зависимости (градуировку
измерительного прибора) осуществляют в соответствии с руководством по
эксплуатации применяемого ИК-фотометра с использованием одного или нескольких
градуировочных образцов, приготовление которых описано выше.
Установление градуировочной зависимости проводят при
замене измерительного прибора, при использовании новой партии четыреххлористого
углерода, либо после длительного перерыва в работе (более 3-х месяцев).
10.9 Контроль
стабильности градуировочной характеристики
10.9.1 Контроль стабильности
градуировочной характеристики проводят каждый раз перед анализом серии проб.
Средствами контроля являются образцы, используемые для установления
градуировочной зависимости согласно 10.8
(не менее 3 образцов).
Градуировочная характеристика
считается стабильной при выполнении условия
(1)
где Хг - результат контрольного измерения
массовой концентрации жиров в градуировочном растворе, мг/см3;
Сг - приписанное значение массовой
концентрации жиров в градуировочном растворе, мг/см3;
d -
допускаемое расхождение между измеренным и приписанным значениями массовой
концентрации жиров, мг/см3 (см. таблицу 2).
Таблица 2 - Допустимые расхождения между измеренными и приписанными
значениями массовой концентрации жиров в образцах при контроле стабильности
градуировочной характеристики
|
Приписанное значение массовой
концентрации жиров образце С, мг/см3
|
Допустимое расхождение d, мг/см3
|
|
0,010
|
0,0024
|
|
0,020
|
0,0048
|
|
0,030
|
0,0072
|
|
0,040
|
0,0096
|
|
0,060
|
0,014
|
10.9.2 Если условие стабильности не выполняется для
одного градуировочного раствора, необходимо выполнить повторное измерение этого
раствора для исключения результата, содержащего грубую погрешность. При
повторном невыполнении условия, выясняют причины нестабильности, устраняют их и
повторяют измерения. Если градуировочная характеристика вновь не будет
удовлетворять условию (1),
устанавливают новую градировочную зависимость.
10.9.3 При выполнении условия (1) учитывают знак разности между измеренными и
приписанными значениями массовой концентрации жиров в образцах. Эта разность
должна иметь как положительное, так и отрицательное значение, если же все
значения имеют один знак, это говорит о наличии систематического отклонения. В
таком случае требуется установить новую градуировочную зависимость.
11 Выполнение измерений
11.1
Холостое измерение
Измерение массовой
концентрации жиров в холостой пробе выполняют одновременно с анализом серии
проб. Для этого берут 0,5 - 1,0 дм очищенной дистиллированной воды и
обрабатывают ее, как описано в 11.2
- 11.4. Результат холостого
измерения вычитают из результата анализа пробы. При высокой величине холостого
определения (превышающей минимально определяемую концентрацию жиров) повторно
проверяют на чистоту используемые реактивы, материалы, посуду и, в случае
необходимости, находят и устраняют причину загрязнения.
11.2
Экстракция
Пробу воды из транспортной склянки целиком переносят в
делительную воронку соответствующей вместимости (не допускается отбор аликвоты
пробы из склянки!). В склянку приливают хлороформ или четыреххлористый углерод
с таким расчетом, чтобы его объем вместе с использованным для консервации пробы
растворителем составил 15 см3.
Тщательно ополаскивают растворителем стенки склянки, в
которой находилась проба, и переносят его в делительную воронку. Выполняют
экстракцию, энергично встряхивая воронку в течение 3 мин.
После расслоения фаз нижний слой (экстракт) сливают в
колбу с притертой пробкой вместимостью 50 см3. Оставшуюся в
делительной воронке пробу воды повторно экстрагируют 10 см3
хлороформа или четыреххлористого углерода. Экстракты объединяют и подвергают
обработке согласно 11.3 или
оставляют на хранение в темном месте. После отделения экстракта измеряют объем
пробы воды в воронке мерным цилиндром.
11.3
Выделение жиров методом тонкослойной хроматографии
Экстракт обезвоживают сульфатом натрия, добавляя его в
колбу небольшими порциями при перемешивании содержимого стеклянной палочкой или
встряхиванием. Добавление сульфата натрия прекращают после полного исчезновения
эмульсии.
Обезвоженный экстракт переносят в стакан вместимостью
50 см3, трижды ополаскивают стенки колбы с сульфатом натрия
небольшими порциями (около 2 см3) хлороформа или четыреххлористого
углерода, которые присоединяют к основной порции экстракта. Экстракт оставляют
в вытяжном шкафу при комнатной температуре для упаривания. После уменьшения
объема экстракта примерно до 2 см3 количественно переносят его в
стаканчик вместимостью 5 - 10 см3, обмывая стенки 0,5 см3
хлороформа или четыреххлористого углерода, и оставляют до полного упаривания.
Остаток растворяют в 0,2 см3 хлороформа или четыреххлористого
углерода, ополаскивая стенки стаканчика.
Подвижную фазу, подготовленную в соответствии с 10.4, наливают в хроматографическую
камеру не менее, чем за 10 мин до начала хроматографирования и оставляют для
насыщения камеры парами подвижной фазы.
Сконцентрированную пробу с помощью капилляра малыми
порциями (по 0,01 - 0,02 см3) наносят на полосу с оксидом алюминия
на расстоянии 6 - 7 мм от края хроматографической пластинки в виде пятна
диаметром не более 2 мм. Пластинку помещают в хроматографическую камеру под
углом от 20° до 30°.
Через 5 мин, когда фронт подвижной фазы достигнет
верхнего края оксида алюминия, пластинку вынимают, и после испарения
растворителя (через 5 - 10 мин) помещают в камеру, предварительно насыщенную
парами йода. Жиры на пластинке образуют коричневые пятна, имеющие величину Rf = 0,45 - 0,55. Границы пятна отмечают скальпелем.
Отмеченный участок, оксида алюминия после исчезновения
паров йода, с помощью скальпеля счищают в воронку с бумажным фильтром. С
помощью градуированной пипетки вместимостью 5 см3 элюируют жиры с
оксида алюминия небольшими (по 2 - 2,5 см3) порциями
четыреххлористого углерода в градуированную пробирку с притертой пробкой
вместимостью 10 см3 и доводят объем элюата жиров растворителем до
10,0 см3.
11.3 Измерение
Помещают элюат жиров в кювету
ИК-фотометра и производят измерение концентрации жиров в элюате в соответствии
с руководством по эксплуатации конкретного прибора.
Если оптическая плотность
элюата и соответственно концентрация жиров в нем выходит за пределы диапазона,
в котором проводилась градуировка, разбавляют элюат и повторяют измерение.
Разбавление элюатов следует проводить таким образом, чтобы концентрации жиров
после разбавления находилась в пределах от 0,040 до 0,060 мг/см3.
11.4
Мешающие влияния
Выполнению измерений массовой концентрации жиров
могут мешать липиды естественного происхождения, но поскольку их концентрации в
водах значительно ниже концентраций жиров антропогенного происхождения, вкладом
естественных липидов обычно пренебрегают.
12 Вычисление и оформление
результатов измерений
12.1 Массовую концентрацию
жиров в анализируемой пробе воды X, мг/дм3,
находят по формуле
(2)
где С - концентрация жиров в
элюате, найденная по показаниям прибора или градуировочной зависимости, мг/см3
(если прибор градуирован в мг/дм3 в формулу следует подставить
величину С/1000);
V1 - объем элюата, см3;
V - объем пробы воды, дм3;
h - степень разбавления элюата; если
разбавление не проводилось h = 1.
12.2 Результат измерений в
документах, предусматривающих его использование, представляют в виде:
Х ± D, мг/дм3 (Р = 0,95), (3)
где ±D - границы характеристики погрешности
измерений для данной массовой концентрации жиров (см. таблицу 1).
Численные значения результата
измерений должны оканчиваться цифрой того же разряда, что и значения
характеристики погрешности; значения характеристики погрешности не должны
содержать более двух значащих цифр.
12.3 Допустимо представлять
результат в виде:
X ± Dл (Р = 0,95) при условии Dл < D, (4)
где ±Dл - границы характеристики погрешности измерений, установленные при
реализации методики в лаборатории и обеспечиваемые контролем стабильности
результатов измерений.
Примечание -
Допустимо характеристику погрешности результатов измерений при внедрении
методики в лаборатории устанавливать на основе выражения Dл = 0,84D с последующим уточнением по мере накопления информации в
процессе контроля стабильности результатов измерений.
12.4 Результаты измерения
оформляют протоколом или записью в журнале, по формам, приведенным в
Руководстве по качеству лаборатории.
13 Контроль качества результатов
измерений при реализации методики в лаборатории
13.1
Общие положения
13.1.1 Контроль качества
результатов измерений при реализации методики в лаборатории предусматривает:
- оперативный контроль
исполнителем процедуры выполнения измерений (на основе оценки погрешности при
реализации отдельно взятой контрольной процедуры);
- контроль стабильности
результатов измерений (на основе контроля стабильности повторяемости,
внутрилабораторной прецизионности, погрешности).
13.1.2 Периодичность оперативного
контроля исполнителем процедуры выполнения измерений, а также реализуемые
процедуры контроля стабильности результатов измерений регламентируются в
Руководстве по качеству лаборатории.
13.2 Алгоритм
оперативного контроля процедуры выполнения измерений с использованием метода
добавок
13.2.1 Контроль исполнителем
процедуры выполнения измерений проводят путем сравнения результатов отдельно
взятой контрольной процедуры Кк с нормативом контроля К. Для
реализации контрольной процедуры в две чистые склянки (проверка на чистоту по 10.2) наливают по 0,50 - 1,0 дм3
анализируемой воды. В одну из склянок вводят добавку ацетонового раствора
тристеарина, приготовленного из аттестованного раствора тристеарина АР-Ж (см.
приложение А). Для приготовления
ацетонового раствора отбирают 5,0 см3 раствора АР-Ж, переносят его в
мерную колбу вместимостью 50 см3, доводят до метки ацетоном и
перемешивают. Массовая концентрация тристеарина в ацетоновом растворе составит
0,10 мг/см3.
Выполняют измерение массовой
концентрации жиров в обеих склянках согласно разделу 11.
13.2.2 Результат контрольной
процедуры Кк, мг/дм3, рассчитывают по формуле
(5)
где X¢ - результат контрольного измерения массовой концентрации
жиров в с известной добавкой, мг/дм3;
Сд - массовая
концентрация добавки жиров, мг/дм3.
13.2.3 Норматив контроля
погрешности К, мг/дм, рассчитывают по формуле
(6)
где и -
значения характеристик погрешности результатов измерений, установленные при
реализации методики в лаборатории, соответствующие массовой концентрации жиров
в пробе с добавкой и рабочей пробе, мг/дм3.
Примечание -
Допустимо для расчета норматива контроля использовать значения характеристик
погрешности, полученные расчетным путем по формулам и с
последующим уточнением по мере накопления информации в процессе контроля
стабильности результатов измерений.
13.2.4 Если результат
контрольной процедуры удовлетворяет условию:
(7)
процедуру анализа признают
удовлетворительной.
При невыполнении условия (7) контрольную процедуру повторяют с
другой пробой воды. При повторном невыполнении условия (7), выясняют причины, приводящие к неудовлетворительным
результатам, и принимают меры по их устранению.
14 Проверка приемлемости
результатов, полученных в условиях воспроизводимости
14.1 Расхождение между
результатами измерений, полученными в двух лабораториях, не должно превышать
предела воспроизводимости R. При
выполнении этого условия приемлемы оба результата измерений и в качестве
окончательного может быть использовано их общее среднее значение. Значение
предела воспроизводимости рассчитывают по формуле
R = 2,77×sR. (8)
14.2 При превышении предела
воспроизводимости могут быть использованы методы оценки приемлемости результатов
измерений согласно ГОСТ
Р ИСО 5725-6 (раздел 5) или МИ
2881.
14.3 Проверку приемлемости
проводят при необходимости сравнения результатов измерений, полученных двумя
лабораториями.
Приложение А
(обязательное)
Методика приготовления аттестованного
раствора жиров АР-Ж
А.1
Назначение и область применения
Настоящая методика
регламентирует процедуру приготовления аттестованного раствора жиров, предназначенного
для установления градуировочной характеристики приборов и контроля точности
результатов измерений массовых концентраций жиров ИК-фотометрическим методом.
А.2 Метрологические характеристики
Аттестованное значение
массовой концентрации жиров в растворе АР-Ж составляет 1,00 мг/см3;
границы погрешности установления аттестованного значения не превышают ±0,021
мг/см3 при Р = 0,95.
А.3 Средства
измерений, вспомогательные устройства, реактивы
А.3.1 Весы лабораторные
высокого (II) класса точности по ГОСТ 24104-2001.
А.3.2 Колба мерная 2-го
класса точности исполнения 2 по ГОСТ
1770-74 вместимостью 50 см3 - 1 шт.
А.3.5 Стаканчик для
взвешивания (бюкс) СВ-19/9 по ГОСТ
25336-82.
А.3.6 Воронка лабораторная по
ГОСТ
25336-82 диаметром 36 мм - 1 шт.
А.3.7 Шпатель по ГОСТ
9147-80.
А.4 Исходные
компоненты аттестованных растворов
А.4.1 Тристеарин по ТУ
6-09-07-926-77, ч., очищенный согласно 10.1.6,
с содержанием основного вещества в препарате не менее 98 %.
А.4.2 Углерод
четыреххлористый по ГОСТ 20288-74,
х.ч., или ТУ 6-09-3219-84, ос.ч.
А.5 Процедура приготовления аттестованного
раствора жиров АР-Ж
Взвешивают в бюксе с
точностью до четвертого знака после запятой 0,050 г очищенного тристеарина.
Количественно переносят навеску в мерную колбу вместимостью 50 см3,
растворяют в четыреххлористом углероде, доводят объём раствора до метки и
перемешивают.
Полученному раствору
приписывают массовую концентрацию жиров 1,00 мг/см3.
А.6 Расчет метрологических характеристик
аттестованного раствора
А.6.1 Аттестованное значение
массовой концентрации жиров в растворе АР-Ж С, мг/см3, рассчитывают
по формуле
(А.1)
где m - масса навески тристеарина, г;
V - вместимость мерной колбы, см3;
А.6.2 Расчет предела
возможных значений погрешности приготовления аттестованного раствора АР-Ж, D, мг/см3, выполняют по формуле
(А.2)
где Dm - предельное значение возможного
отклонения массовой доли основного вещества в реактиве от приписанного значения
m;
m - массовая доля основного вещества
(тристеарина) в реактиве, приписанная реактиву;
Dm - предельная возможная погрешность
взвешивания, г;
m - масса навески тристеарина, г;
Dv - предельное значение возможного
отклонения вместимости мерной колбы от номинального значения, см3.
Предел возможных значений
погрешности приготовления аттестованного раствора АР-Ж равен
А.7
Требования безопасности
Приготовление раствора АР-Ж
необходимо проводить при включенной вытяжной вентиляции. Содержание
четыреххлористого углерода в воздухе рабочей зоны не должно превышать
установленных предельно допустимых концентраций в соответствии с ГОСТ
12.1.005.
А.8 Требования к квалификации операторов
Аттестованный раствор может
готовить инженер или лаборант со средним профессиональным образованием, прошедший
специальную подготовку и имеющий стаж работы в химической лаборатории не менее
6 мес.
А.9 Требования к маркировке
На склянку с аттестованным
раствором должна быть наклеена этикетка с указанием условного обозначения
раствора, величины массовой концентрации жиров, погрешности ее установления и
даты приготовления раствора.
А.10 Условия хранения
Аттестованный раствор АР-Ж,
следует хранить в холодильнике плотно закрытой склянке из темного стекла не
более 3 мес.