МИНИСТЕРСТВО ГЕОЛОГИИ СССР
всесоюзный научно исследовательский институт
МИНЕРАЛЬНОГО СЫРЬЯ (ВИМС)
Выписка из приказа ГГК СССР ft 229 от 18 мая 1964 года
7. Министерству геологии и охраны недр Казахской ССР, главным управлениям и управлениям геологии и охраны недр при Советах министров союзных республик, научно-исследовательским институтам, организациям и учреждениям Госгеолкома СССР:
а) обязать лаборатории при выполнении количественных анализов геологических проб применять методы, рекомендованные ГОСТами, а также Научный советом, по мере утверждения последних ВИКСом.
При отсутствии ГОСТов и методов, утвержденных ВИМСом, разрешить временно применение мотодик, утвержденных в порядке, предусмотренном приказом от I ноября 1954 г. ft 998;
в) выделить лиц, ответственных за выполнение лабораториями установленных настоящим приказом требований к применению наиболее прогрессивных методов анализа.
Приложение ft 3, § 8. Размножение инструкций на местах во избежание возможных искажений разрешается только фотографическим или электрографическим путем.
К? 85-х
ФОТОМЕТРИЧЕСКИЙ МЕТОД ОПРЕДЕЛЕНИЯ ФТОРА В ГОРНЫХ ПОРОДАХ ПО ОСЛАБЛЕНИЮ ОКРАСКИ РАСТВОРА КОМПЛЕКСА ТОРИЯ С АРСЕНАЗО х}
Сущность метода
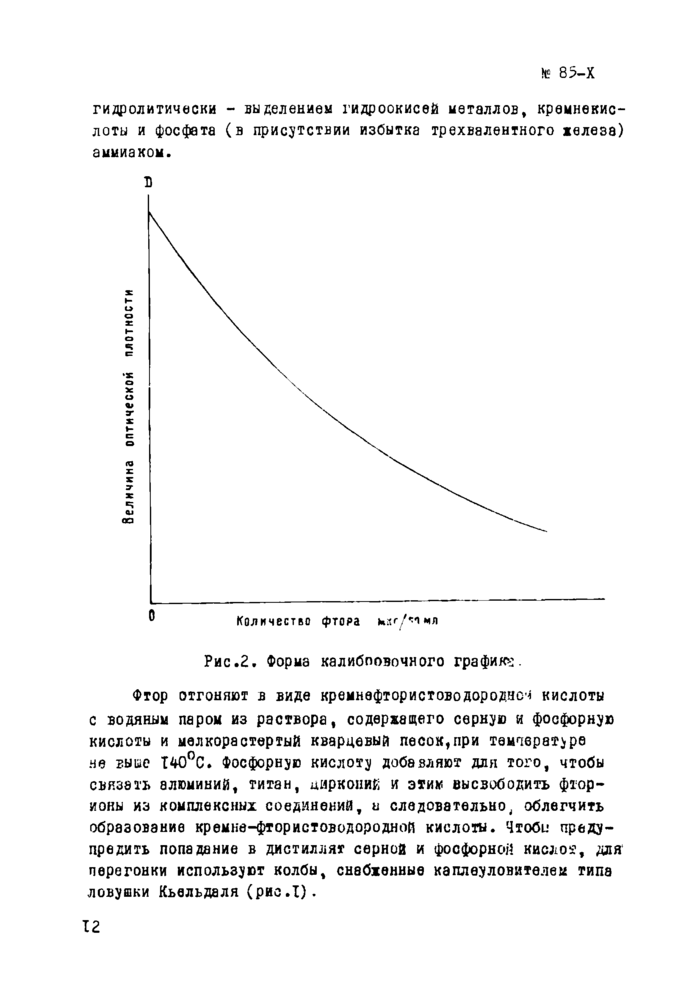
Определение фтора основано на его способности образовывать с торием бесцветный фторидный комплекс, более прочный, чем окрашенный комплекс о арсеназо I* По степени ослабления окраски комплексного соединения тория с арсеназо I судят о количестве фтора, вошедшего в реакцию с торием Реакцию проводят в растворе, pH которого равен 2. Окраска раствора ослабевает тотчас хе после прибавления фтор-ионов. Оптическая плотность растворов не подчиняется закону Бугера-Беера. График зависимости оптической плотности от концентрации фтора представляет собой вогнутую линию (рис.2). Максимум оветопоглощения комплекса тория с арсеназо находится в области 570-58D ммк. Обнаруживаемый минимум составляет 0,01— 0,02 мкг/мл фтора.
Определению фтора мешают: I. Элементы, образующие окрашенные соединения с арсеназо при pH =2 (налр., железо Ш, алю-*-миний, цирконий, титан, уран Л, редкоземельные элементы, вольфрам); 2. Элементы, связывающие в комплексные соединения фтор (алюминий, титан, цирконий); 3. Анионы, при взаимодействии которых с торием образуются труднорастворимые или комплексные соединения (фосфаты, сульфаты).
Интенсивность окраски комплекса тория с арсеназо снижается в присутствии большого количества солей и в том числе солей щелочных металлов, которые влияют на "ионную силу" раствора.
Мешающее действие сопутствующих элементов устраняется отгонкой фтора в виде кремнефтористоводородьой кислоты или
Внеоена в НСАМ Химико-аналитической лаборатории ВСЕГЕИ,1Э68.
II
te 85-Х
гидролитически - выделением гидроокисей металлов, кремнекис-лоты и фосфата (в присутствии избытка трехвалентного железа) аммиаком.
|
Ъ |
|
|
Рис.2. Форма калибровочного график*:. |
Фтор отгоняют в виде кремнефтористоводороднсч кислоты с водяным паром из раствора, содержащего серную и фосфорную кислоты и мелкорастертый кварцевый песок,при температуре не гыыс Х^О°С. Фосфорную кислоту добавляют дли того, чтобы связать алюминий, титан, цирконий и этим высвободить фтор-ионы из комплексных соединений, и следовательноt облегчить образование кремне-фтористоводородноп кислоты. Чтоби предупредить попадание в дистиллят серной и фосфорной кислот, для перегонки используют колбы, снвбженные каплеуловителем типа ловушки Кьельдаля (рис.1).
12
* 85-Х
Отгонке фтора мешает гелеобразная кремневая кислота, выделяющаяся из раствора в осадок и захватывающая часть фто-ра.
Гидролитическое отделение мешающих элементов осаждением аммиаком следует применять для пород, содержащих не более I» фтора; при более высоком содержании фтор может частично задерживаться осадком гидроокисей, либо удерживать в раство** ре алюминий, который затем переходит в фильтрат. Этот способ не применим также при определении фтора в породах, содержащих сульфаты: при осаждоиии гидроокисей аммиаком сульфат-ионы проходят в фильтрат вместе со фтором и мешают определению.
Для разложения природных материалов применяют, в зависимости от их состава, различные иетоды. При анализе фосфатов и фторкарбонатов пробу разлагают кислотоми непосредственно в процессе отгонки. Породы, неразлагаемые кислотами и содержощг.е в навеске не более 40-50 мг кремкекислоты, раз-»* лагают сплавлением с содой. Породы, содержащие большие количества кремнекислоты и более 0,5» фтора, спекают с двукратным количеством карбоната калия-натрия: при обработке спека водой кремнекислота переходит в форму, не способную к пепти-зациит . Породы, содержащие большие количества кремнекислоты и не более 0,5% фтора, можно сплавлять с карбонатом калия-натрия с добавлением окиси цинка: после выщелачивания сплава водой силикат цинка остается в нерастворимом остатке. Сульфидные породы сплавляют с перекисью натрия. Если при перегонке присутствуют небольшие количества сульфидов, то в дистилляционную колбу вводят окислитель-перманганат калия.
Фотоколориметрический метод предназначается для определения фтора при содержании его от 0,02 до 5* в силикатных породах, фосфоритах, фторкарбонатах и сульфидах. Для отделения от мешающих компонентов используется отгонка фтора; при содержании фтора не более 1,0» может быть применено гидролитическое отделение.
V 8>-X
Погрешность определения при содержании фтора от 0,05 до Ъ% укладывается в допустимые расхождения (см. табл Л). При содержании фтора от 0,02 до 0,05% расхождение между параллельными определениями не превышает 60% отн. (по опыту работы лаборатории).
Таблица 2
|
Содержание фтора, абс.^ |
| Допустимые расхождении отн. % |
|
2 - 4,99 |
18 |
|
I - 1,99 |
20 |
|
0,Ь - 0,99 |
30 |
|
0,2 - 0,499 |
37 |
|
0,1 - 0,199 |
46 |
|
0,05 - С,099 |
49 |
Допустимые расхождения 2
Реактивы и материалы
1. Кислота серная, разбавленная 1:1 и 2:1
2. Кислота соляная, разбавленная 1:1 и 1:100
3. Кислота фосфорная , d 1,70*^
4. Аммиак, 253/6-ный раствор и разбавленный 1:10
5. Аммоний хлористый, 2с^-ный нейтральный растер.
6. Железо хлорное ( &С-з)* 25г/6-ныЯ раствор.
7. Калий марганцовокислый, I^-ный раствор.
3. Натрий углекислый, безводный и З^ный раствор. 9. Натрий-калий углекислый.
10.Окись цинка.
II.Перекись натрия.
Т2.Арсеназо-1, O.OS'Jb-Hbip. раствор
относительная плотность
I и
То«Стандартные растворы ^тора.
Раствор ь. Навеску чистого сухого фтористого натрия 0,221 г растворяют в Т л дистиллированной воды. I иг раствора А содержит ТОО икг фтора.
.Раствор Б. 1иО мл раствора А доливают водой до I л.
I мл раствора Б содержит 10 мкг фтора.
Растворы хранят в сосудах из полиэтилена.
H. Стандартный раствор тория. I г азотнокислого тория (ТН0»г0з\-4н2О ) растворяют в I л воды. Т*.тр раствора устанавливают весовым методом. Разбавляй полученный раствор, готовят раствор, содержащий 30 ыкг тория в I мл. На каждые 100 мл последнего растворе добавляют I мл соляной кислоты
Ct 1,19.
15. Бумага индикаторная " лакмусовая".
16. Индикатор (К - динитрофенол, насыщенный водный раствор.
17. Песок кварцевый, истертый до 200 меш.
Аппаратура Прибор для отгонки фтора (см.рис.Х)
I. Колба перегонная (Б) емкостью 150-250 мл, снабженная каплеуловителем типа ловушки Кьельдаля и муфтой для термометра •
2. Колба емкос1Ы) I л (.л) (парообразователь).
3. Холодильник шариковый.
Колбонагреватели электрические (два).
5. Термометр химический С-<г50иС.
Ход анализа Разложение материала и обгонка фтора А. Разложение
I. Породы, разлагаемые кислотами (фосфаты, фгоркарбо-наты). Навеску 0,1 - 0,2 г помещают в перегонную нолоу
№ 85-Х
(рисЛ)и смывают весовое стекло 20-30 мл воды.Если присутствует небольшое количество сульфидов, прибавляют немного перманганата калия. Проба разлагается одновременно с отгонкой Фтора.
2. Породы, нераэлагаемые кислотами и содеркаме не более 40-50 мг кромнекислоты в наьеске. Навеску 0,1 - 0,2 г смешивают в платиновом тигло с 2-3 г соды и сплавляют до прекращения выделения пузырьков. Сплав выщелачивают водой, затем, не отфильтровывая осадка, нейтрализуют на холоду серной кислотой 1:1 и помещают в нерехонную колбу, b присутствии небольшого количества сульфидов в перегонную колбу прибавляют перманганат калия до неисчезаюцей розовей окраски.
3. Породы, содержащие большие количества кремнекислоты и более Q.5-* Фтора. Навеску 0,5-1,0 г смешивают в платиновом тигле с двукратным количеством углекислого калин-натрия и спекают при 500°С в течение часа. Остывший спек переносят в стакан и далее поступают как при сплавлении с содой.
4. Породы, содержащие большие количества кремнекислоты и менее 0.5* фтора. Невеску 0,5 г тщательно смешивают в платиновом или никелевом тигле с 0,6 г окиси цинка и 3-4 г безводного карбоната калия-натрия. Сначала сплавляют в течение 15 минут на слабом пламени, а затем 15-20 минут при 750°С.
При сплавлении в платиновом тигле следует обеспечить окислительную среду, чтобы нс испортить тигель. Сплав выщелачивают водой, раствор фильтруют и осадок промывают несколько раз 3*-ным раствором соды. Фильтрат нейтрализуют на холоду серной кислотой 1:1 и переносят в перегонную колбу.
5. Счлывидные породы. Навеску 0,5-1,0 г смешивают в никелевом тигле тонкой стеклянной палочкой с 3 г сухой не-разлокившейся ^желтой) перекиси натрия. Сверху насыпают тонкий слой перекиси натрия и. нагревают для удаления влаги на электрической плитке с открытой спиралью. Затем смесь сплавляют в пламени горелки или в специально отведенной для этого муфельной печи, повышая температуру постепенно во избежание разбрызгивания. Доводят температуру до 600-700°С и вы-министерство гко.югии ссср
Научный Совет по аналитическим методам при ВИМСе
Химико-аналитические методы
Инструкция №85 X
ОБЪЕМНОЕ ОПРЕДЕЛЕНИЕ ФТОРА ТИТРОВАНИЕМ НИТРАТОМ ТОРИЯ С ПРЕДВАРИТЕЛЬНОЙ ОТГОНКОЙ В ВИДЕ КРЕМНЕФТОРИСТОВОДОРОДНОЙ КИСЛОТЫ
Всесомыиый научно-исследовательский институт минерального сырья
(ВИМС)
МОСКВА, 1969 г.
J.: 85-Х
Для отделения от мешающих элементов фтор отгоняют в виде кремьефтористоводородной кислоты при температуре не выше 140°С| в присутствии измельченного кварца и разбавленной сорной кислоты^* . Чтобы избежать при перегонке мешающего действия алюминия, циркония, титана, образующих комплексные соединения со утором, к раствору прибавляют фосфорную кислоту.
Отгонке фтора мешает гелеобразная кремневая кислота, выделяющаяся из растворов в осадок и захватывающая часть фтора.
При анализе кислоторастворимых материалов (фосфориты), не содержащих разлагаемых кислотами силикатов, «/гор отгоняют непосредственно из навески. Породы, содержащие в навеске не более 40 мг кремнекислоты (топаз, флюориты), разлагают сплавлением с содой. Породы, богатые кремиекислотой, спекают с двукратным количеством карбоната кэлия-натрия и спек обрабатывают водой. При обработке спека водой кремневая кислота яе пелтизируется^. Пробы, содержащие органическое вещество, предварительно обжигают в фарфоровых тиглях при 500°С в тече*-ние часа*. Сульфидные породы сплавляют с перекисью натрия.
Если в породе присутствуют небольшие количества сульфидов, го в дистилляционную колбу вводят окислитель-перманганат калия.
Метод рекомендуется для анализа горных пород и минералов при содержании фтора 2,Oi и выше. Таблица I
Допустимые расхождения^
|
Содержание фтора, it |
; Допустимые расхождения I отн. ъ |
|
50-59,99 |
2,4 |
|
40-49,99 |
2,8 |
|
30-39,99 |
5,7 |
|
20-29,99 |
4,6 |
|
10-19,99 |
7,3 |
|
5- 9,99 |
II |
|
2- 4,99 |
ТВ |
Реактивы и материалы
1. Кислота серная, разбавленная 1:1. Серкую кмолоту dX,84x^ нагревают до появления густых паров, охлаждают и
разбавляют до нужной концентрации, вливая киолоту в воду.
2. Кислота соляная, 0,1 н. раствор.8,23 мл соляной кислоты d 1,19 доливают водой до I л.
3. Кислота фосфорная (орто), d 1*7.
4. Натр едкий, Il^-ный иОТ н.растворы (4 г едкого натра в I л воды).
5. Калий-натрий углекислый.
6. Натрий углекислый.
7. Перекись натрия.
8. Буферный раствор. 2С0 мл X М раствора монохлор>ксус-ной кислоты нейтрализуют раствором едкого натра по фенолфталеину, прибавляют еще 200 мл I М раствора моыохлорукусусыой кислоты и доливают водой до X л. Величину pH раствора проверяют на pH-метре и,если она не укладывается в установленный интервал (2,9 - 3,Х), то прибавляют понемногу ХО н. раствор едкого натра, доводя pH буферного растворе до 3.
9. Торий азотнокислый, 0,05 н.титрованный раствор.
6,9 г азотнокислого тория (ТН(а/05)4 4 И20 ] растворяют
в воде, раствор фильтруют в мерную колбу на X л и доливают водой до метки. I мл раствора соответствует и,95 мг фтора.
Титр раствора азотнокислого тория устанавливают по чистому фтористому натрию в условиях определения или весовым путем -взвешиванием ThQs.
Гитр азотнокислого тория при весовом определении рассчитывают по формуло
А . U.2877 Б
где А - вес осадка окиси тория, г;
Б - объем растворе азотнокислого тория, взятого для осаждения, мл.
d - относительная плотность.
* 85-Х
',2877 - коэффициент пересчета окиси тория на фтор.
ТО. Натрий фтористый, стандартный растнор. 2,21 г дваж-» ды перекристаллизованного и высушенного при 105-П0°С фтористого натрия растворяют в свежелерегнанной дистиллированной воде в мерной колбе на I л и доливают водой до метки.
I мл раствора содержит I мг фтора.
11. Бумага лакмусовая.
12. Натрий ализаринсульфововокислый (ализарин 5 ),
0,1*-ный раствор.
13. Фенолфталеин, 1>-ныЙ раствор в 60*-ном этиловом спирте.
14. Песок кварцевый, истертый до 200 меш.
Аппаратура Прибор для отгонки фтора (рио. I)
1. Колба перегонная (Б) емкостью 150-250 мл, снабженная каплеуловителем типа ловушки Кьельдаля и муфтой для термометра.
2. Колба емкостью I л (А) (парообразователь).
3. Холодильник шариковый.
4. Колбонагреватеди электрическио (два).
5. Термометр химический 0-250°С.
Ход анализа Разложение материала
I. Породы, оаалягвамыв кислотами (Фосфаты, фторкарбо-на ты). Навеску 0,5-1,0 г помещают в перегонную колбу, приливают 30 мл воды и отгоняют фтор как описано ниже.
Породы, неразлагаемые кислотами и содержащие не более 40-50 мг кромнекислоты в невеске. Навеску 0,1-0,2 г смешивают в платиновом тигле с 2-3 г соды и сплавляют до пре -крещения выделения пузырьков газа.Сплав выщелачивают в ста-
6
V» 85-х
кан 10-20 мл горячей воды и слабо нагревают до распадения. Содержимое стакана охлаждают, нейтрализуют оерной кислотой 1:1, прибавляя ее по каплям до прекращения выделения углокислого газа, переносят в перегонную колбу и обмывают стакан небольшими порциями воды. Общий объем жидкости в перегонной колбе должен составлять 35-40 мл.
3. Породы. содэрхиаие большие количества кряиьекислоты. Навеску 0,5 - 1,0 г смешивают в платиновом тигле с двукратным количеством углекислого калия-натрия и спекают при 500°С в течение часа. Остывший спек переносят в стаквн и далее поступают как при сплавлении с содой.
4. Сульфидные породы. Навеску 0,5-1,0 г смешивают в никелевом тигле тонкой стеклянной палочкой с 3 г сухой не-разложившейся (желтой) перекиси натрия. Сверху насыпают тонкий слой перекиси натрия и нагревают для удаления влаги на электрической плитке с открытой спиралью. Затем смесь сплавляют в пламени горелки или в специально отведенной для этого муфельной печи, повышая температуру постепенно, во избежание разбрызгивания. Доводят температуру до 600-700°С и выдерживают при спокойном плавлении 5-10 минут. Тигель охлаждают, сплав выщелачивают водой, раствор нейтрализуют на холоду серной кислотой 1:1 и помещают в перегонную колбу.
Отгонка фтора
В перегонную колбу, в которую помещена навеска или переведенная в раствор проба,вносят40 мл серной кислоты 1:1, 2 мл фосфорной кислоты cL 1,7, 0,1-0,2 г кварцевого песка и Несколько крупинок пористого стекла*^ для предотвращения толчков при кипении. Колбу закрывают пробкой, соединенной с холодильником. Парообразователь наполняют водой более, чем наполовину, и помещают на дно также несколько крупинок пористого стекла. Парообразователь и перегонную колбу нагревают на электрических колбонагревэтелях. Приемником служит стакан емкостью 400-500 мл.
Пористое стекло приготовляется дроблением пористых пластинок из бракованных стеклянных тиглем
*>
Я» 83-х
Кожбу с водой нагревают до кипения, выпуская образующийся пар в воздух С зажим "а" закрыт, зажим "в" открыт;. Нагревают дмстилляционную колбу до 125-Т30°С и затем пропускают в нее пар, открывая *>ажим “а" и закрывая важны "в".
Поддерживая температуру в перегонной колбе 1<*0+5°С, отгоняют фтористоводородную кислоту с водяным паром до тех пор, пока в приемнике соберется 230-350 мл дистиллята.
Рис Л. Прибор для отгонки кремнефтористоводородной кислоты с водяным паром.
Объемное определение фтора
Дистиллят нейтрализуют по фенолфталеину 0,1 н. раствором едкого натра, переносят раствор в мерную колбу на 500 мл и доливают водой до метки.
При низком содержании фтора объем дистиллята предварительно сокращают. Для этого его нейтрализуют IO^-ным раствором едкого натра до посинения лакмусовой бумаги и выпаривают
* 85-Х
в платиновой чашке до 50 мл, следя за тем, чтобы раствор сохранил щелочную реакцию. Упаренный дистиллят можно также перенести в мерную колбу на 10С мл и долить водой до метки.
Для определения фтора отбирают аликвотную часть раствора 50 мл, прибавляют 5 капель 0,1*-ного раствора ализарин-сульфоната и 0,1 н.раствор соляной кислоты точно до исчезновения розового окрашивания индикатора. Прибавляют 2,5 мл буферного раствора и титруют 0,05 н. раствором азотнокислого тория, прибавляя его по каплям, при перемешивании, до появления розовой окраски.
Вычисление результатов анализа» Содержание фтора в исследуемом материале вычисляют по формуле:
£р= —- . ТОО
где: Т - титр раствора азотнокислого тория, вырвженный в граммах фтора;
О - объем раствора азотнокислого тория, пошедшего на титрование, мл;
Н - навеска, соответствующая аликвотной части испытуемого раствора, взятой для титрования, г.
Литература
1. Бочарова А.П. Методы определения фторе. Научно-методические и производственные материалы лабораторий Министерства геологии, ВИМС, бюллетень * 10 (102), 1951, стр.9.
2. Гиллебранд В.Ф., Лендель Г.Э., Брайт Г.А., Гофман Д.И. Практическое руководство по неорганическому анализу. Госхим-издат, 1957, стр. 756.
3. Данилова В.В. К геохимии рассеянного фтора. Труды Биогеохимической лаборатории АН СССР, УП, 76, 1944.
Выпаривать подщелоченный дистиллят в стеклянной или фарфоровой чашке нельзя, т.к.при этом получаются пониженные результаты^.
с
fr 85-Х
4. Инструкция по внутрилабораторному контролю точности (воспроизводимости) результатов количественных анализов рядовых проб полезных ископаемых, выполняемых в лабораториях Министерства Геологии СССР, 1968 г.
Методы химического анализа минерального сырья, вып.
8, Изд-во "Недра", 1965, стр.241.
6. Шарло г. Методы аналитической химии. Количественный анализ неорганических соединений. "Химия", 1966, стр.885.
7. Willard Н.Н.,Winter О.В. Volumetric method for determination of fluorine. Jhd.EnM.chem.Anal.Ed, 5,7 (1953);CM. также Z.anal.&iem.96,213 (1934).
ТП